
Horas después de que la Argentina superara las 50.000 muertes por COVID-19, Infobae confirmó que el próximo miércoles por la madrugada llegarán al país una primera tanda de 580.000 dosis de la vacuna Covishield, una variante de la fabricada por AstraZeneca/Oxford, pero producida por el Serum Institute de la India, mediante un acuerdo de colaboración en el contexto de una transferencia de tecnología del laboratorio anglosueco y la universidad británica. Según pudo conocer este medio, el segundo envío de otras 580.000 dosis llegarían en marzo provenientes también de la India en una aerolínea privada.
La noticia tiene gran relevancia para nuestro país en momentos en que se está aplicando solamente la vacuna rusa Sputnik V solamente al personal de la salud sin haber logrado hasta ahora un suministro lo suficientemente importante y fluido de arribos como para aplicarlas masivamente. En un país que está frente al escenario de estrangulamiento de llegada de vacunas debido a la demanda global, el Gobierno podría decidir, en lo que sería una nueva estrategia epidemiológica, que la vacuna Covishield se aplique en una sola dosis (estrategia one shot), ya que los últimos análisis efectuados por el laboratorio AstraZeneca probaron que en una sola aplicación la misma alcanza el 76% de eficacia contra el nuevo coronavirus SARS-CoV-2; un porcentaje de protección suficientemente bueno, según establece la Organización Mundial de la Salud (OMS) para una inoculación viral efectiva de este tipo de virus.
Cabe aclarar que el 30 de diciembre de 2020, la Administración Nacional de Medicamentos, Alimentos y Tecnología Médica (ANMAT) validó la vacuna AZD1222 de Oxford/AstraZeneca en Argentina bajo uso de emergencia contra el virus SARS-CoV-2 en dos dosis, al considerar que “presenta un aceptable balance beneficio-riesgo”,permitiendo sustentar el otorgamiento de la inscripción y autorización condicional del producto para la indicación solicitada. La misma se otorgó por el plazo de un año contado a partir de la fecha de la presente disposición, bajo la condición de venta bajo receta”.
Esta vacuna, la primera creada contra el SARS-COV-2 en el mundo luego de que estallara la pandemia global, sirve para la inmunización activa de personas mayores de 18 años con dos dosis administradas con un intervalo de entre 4 y 12 semanas, según recomendó en primer lugar la agencia regulatoria inglesa (MHRA) al autorizarla como suministro de emergencia asegurando que en los ensayos clínicos de Fase III se demostró que este régimen es seguro y eficaz para prevenir el COVID-19 sintomático, sin casos graves ni hospitalizaciones más de 14 días después de la segunda dosis, con la que se alcanza un 82% de protección.
De esta manera, las autoridades sanitarias evaluarían si las 580.000 dosis servirán para inmunizar a 290.000 personas con dos dosis, o bien a 580.000 personas con una sola dosis. Según las previsiones pautadas, en marzo el país recibiría una segunda tanda también de 580.000 dosis.
Ayer, de que llegara al país la tercera entrega de vacunas Sputnik V, en un nuevo vuelo de Aerolíneas Argentinas, el ministro de Salud de la Nación, Ginés González García, anticipó a sus colegas provinciales y de CABA la llegada de las vacunas desde India la próxima semana para reforzar la campaña de vacunación al personal de la salud y así, pasar luego a la fase vacunatoria de mayores de 70 años.
“La buena noticia es que tenemos más vacunas. A las vacunas que llegan hoy [por ayer] -400.000 dosis de la vacuna Sputnik V- hay que sumarles las que están llegando a principios de la semana que viene desde India para cubrir a todos los trabajadores de salud y comenzar a vacunar a las personas mayores de 70 años”, detalló González García en la reunión con los ministros de las 24 jurisdicciones del país, en el marco del Consejo Federal de Salud (Cofesa).

El Ministro celebró que los próximos ingresos de vacunas contra la COVID-19 “permitirán escalar la vacunación de los grupos priorizados”. Además anunció que el Banco Mundial otorgó una financiación adicional por 250 millones de dólares para transferencias directas a las provincias “en el marco del cumplimiento de metas del Programa Sumar”.
El martes 9 de febrero, el Ministerio de Salud de la Nación autorizó con carácter “de emergencia” la vacuna Covishield producida en India para combatir la enfermedad COVID-19, después de que la Administración Nacional de Medicamentos, Alimentos y Tecnología (Anmat) diera luz verde a su aprobación a través de un informe técnico, con el mismo mecanismo que se utilizó para la llegada de la Sputnik V, el 23 de diciembre de 2020. Además, se espera para marzo la llegada de otra tanda de 580.000 dosis desde India.
Estas dosis se agregarán a las 23,6 millones (habían sido 22,4 millones originalmente y se le sumaron 1,2 millones más en un convenio suscripto en febrero), que el Gobierno ya contrató con el laboratorio anglosueco en producción conjunta con la biotecnológica local mAbxience y la mexicana Liomont y que se está fraccionando y envasando en México, para ser distribuida en toda la región desde marzo.

Según precisaron en la resolución 627/2021, publicada en el Boletín Oficial del martes, las dosis que arribarán la semana próxima son de la “vacuna COVISHIELD/ ChAdOx1nCoV-19 Corona Virus Vaccine – Recombinant producida por el Serum Institute de la India”, en colaboración con la Universidad de Oxford y AstraZeneca.
Se trata de una vacuna elaborada bajo transferencia de tecnología del laboratorio AstraZeneca y la Universidad de Oxford, cuyo inmunizante ya había aprobado la Argentina el 30 de diciembre pasado. En este caso, su aprobación se centró en “determinar que dicha transferencia (de tecnología) no impacta en la calidad, seguridad y eficacia” del producto que ya ha sido aprobado por 12 países, además de la autoridad sanitaria de India.
El decreto indica que “no se han presentado eventos adversos graves ni se han identificado diferencias significativas en la eficacia observada en los diferentes grupos etarios que participaron de los ensayos clínicos”.
Los resultados demostraron una eficacia de la vacuna del 76% (IC: 59% a 86%) después de una primera dosis, con la protección mantenida hasta la segunda dosis. Con un intervalo entre dosis de 12 semanas o más, la eficacia de la vacuna aumentó al 82% (IC: 63%, 92%).

El análisis también mostró el potencial de la vacuna para reducir la transmisión asintomática del virus, según los hisopados semanales obtenidos de voluntarios en el ensayo del Reino Unido. Los datos mostraron que las lecturas de PCR positivas se redujeron en un 67% (IC: 49%, 78%) después de una dosis única y en un 50% (IC: 38% a 59%) después del régimen de dos dosis, lo que respalda un impacto sustancial en la transmisión del virus.
El resultado principal de la eficacia se basó en 17.177 participantes que acumularon 332 casos sintomáticos de los ensayos de fase III del Reino Unido (COV002), Brasil (COV003) y Sudáfrica (COV005), dirigidos por la Universidad de Oxford y AstraZeneca; 201 casos más que los informados anteriormente.
El Gobierno tiene contratos de provisión de vacunas contra el COVID-19 por unas 62 millones de dosis de distintos laboratorios, según explicó el ministro Ginés González recientemente ante una comisión legislativa.
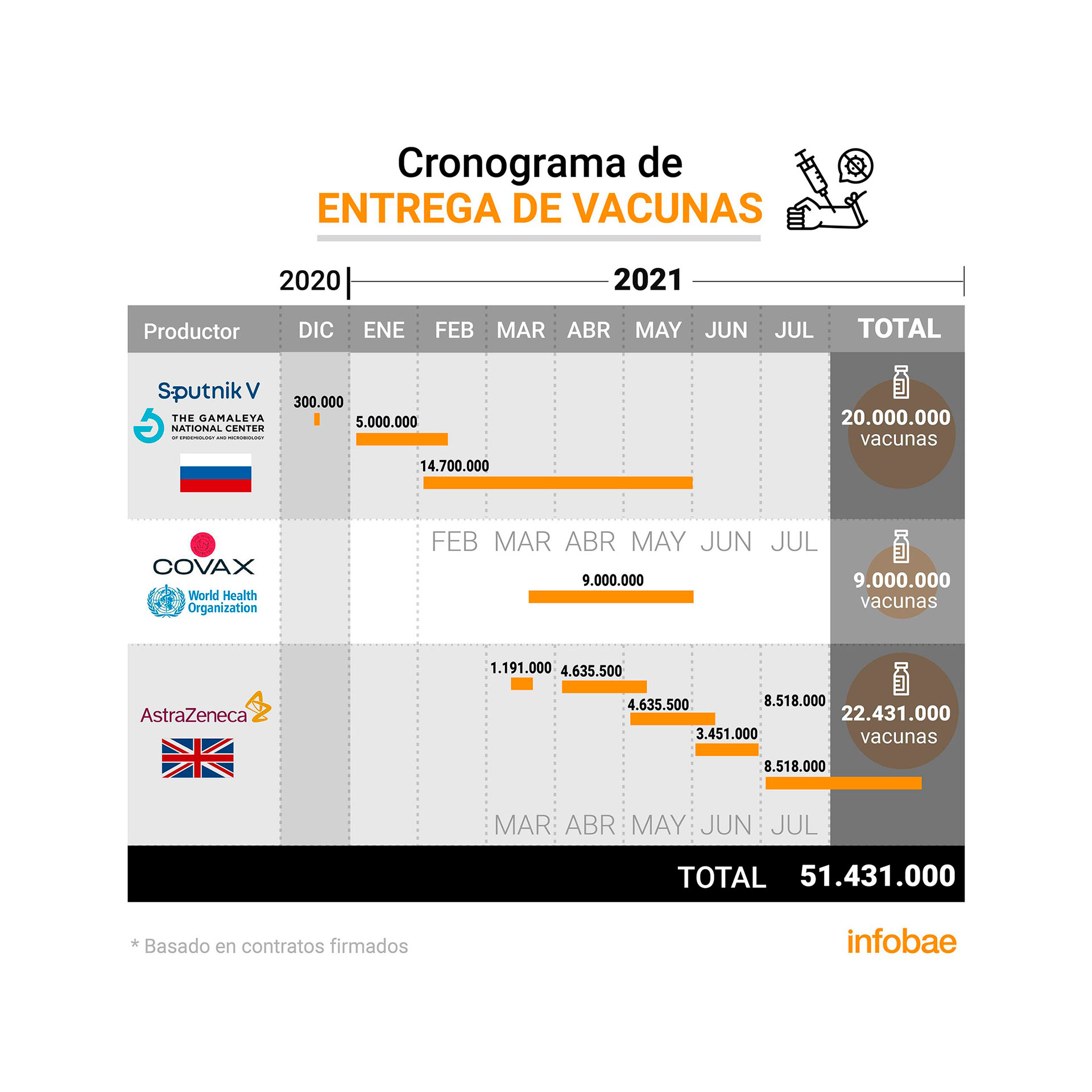
El ministro precisó que Argentina tiene acuerdos para recibir 30 millones de dosis de Sputnik V, 23,6 millones de AstraZeneca y nueve millones por el mecanismo Covax, una iniciativa internacional para garantizar una distribución justa de los medios contra el COVID-19. Según esos datos, el funcionario afirmó que el gobierno espera imnunizar a toda la población argentina mayor de 18 años.
SEGUÍ LEYENDO:
Últimas Noticias
Cómo detectar y prevenir la pérdida de audición: las principales señales de alerta
En el marco de una efeméride en Argentina, un repaso sobre cómo el diagnóstico precoz permite evitar complicaciones. La importancia de los chequeos regulares y la protección frente al ruido excesivo

Cuáles son los alimentos más ricos en vitaminas y minerales y por qué son clave para prevenir enfermedades
Una selección variada de productos de origen natural permite obtener micronutrientes esenciales que fortalecen el organismo, ayudan a evitar carencias y optimizan funciones biológicas clave, según especialistas

Fiebre Oropouche: cuáles son los síntomas y cómo el virus se expande más allá de Sudamérica
Afecta a personas de todas las edades y puede pasar desapercibido por la falta de signos graves. El líder de dos nuevos estudios contó a Infobae por qué la aparición de la infección en nuevos territorios alerta a la comunidad científica

Atragantamiento en menores: por qué es una de las principales causas de muerte accidental y cómo prevenirlo
Especialistas advierten que la mayoría de los casos es prevenible con supervisión adecuada durante las comidas y saber cómo actuar de inmediato ante una emergencia

Beber agua antes de comer no garantiza una mayor pérdida de peso
Aunque esta costumbre se ha extendido como un truco, las investigaciones muestran que su impacto suele ser discreto y a menudo temporal






