Durante años, los científicos observaron una relación entre la inflamación persistente y el desarrollo de tumores, pero no lograban explicar con precisión qué ocurría a nivel celular. ¿Cómo un episodio aparentemente superado puede influir en la aparición de una patología mucho tiempo después?
Una investigación reciente aporta una respuesta: esos eventos no desaparecen por completo, sino que dejan señales duraderas en las células.
Un equipo del Broad Institute of MIT and Harvard identificó un vínculo molecular entre inflamación intestinal crónica y mayor probabilidad de desarrollar cáncer colorrectal. El trabajo, publicado en la revista Nature, demuestra que estos procesos generan “cicatrices” en el epigenoma, un sistema que regula la activación de los genes sin modificar la secuencia del ADN.
Una huella que permanece aun cuando el tejido se recupera
Aunque el intestino puede regenerarse tras un episodio inflamatorio, la investigación muestra que ciertas células conservan una memoria biológica. Estas marcas no alteran el ADN, pero sí cambian la forma en que se utiliza la información genética.
Para entenderlo, puede pensarse en el material genético como un manual de instrucciones. Todas las células contienen el mismo contenido, pero no todas usan las mismas páginas. El epigenoma actúa como un sistema que señala qué partes deben activarse. Cuando hay inflamación prolongada, ese mecanismo puede quedar alterado.

Estas modificaciones pueden mantenerse durante años y dejar a las células en una situación más vulnerable frente a cambios posteriores. En otras palabras, aunque el tejido luzca normal, algunas unidades ya fueron condicionadas por experiencias previas.
“Hemos demostrado que los cambios epigenéticos son la pieza que faltaba para entender cómo la inflamación conduce al cáncer”, explicó Jason Buenrostro, autor principal del estudio.
Doble mecanismo molecular en el cáncer colorrectal
El trabajo propone un modelo que ayuda a entender el mecanismo. En primer lugar, la inflamación deja una marca persistente. Luego, si aparece una mutación, ese contexto previo facilita el crecimiento tumoral.
En ensayos con modelos animales, los investigadores observaron que tejidos con antecedentes inflamatorios desarrollaban tumores más grandes y con mayor velocidad de crecimiento que aquellos sin ese historial.
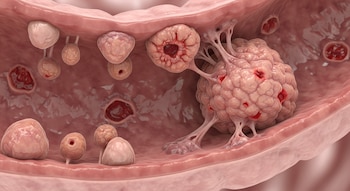
Incluso cuando parecía haber recuperación, algunas células conservaban esa memoria. “Estos factores son transitorios, pero pueden afectar el riesgo de cáncer durante toda la vida”, señaló Surya Nagaraja, primer autor del estudio.
Además, se observó que las células madre transmiten estas marcas a nuevas generaciones, lo que consolida linajes con mayor predisposición a desarrollar tumores. “No todos los que portan mutaciones relacionadas con el cáncer llegan a desarrollar la enfermedad, porque influyen tanto la historia epigenética de la célula como su entorno”, puntualizó Buenrostro.
Implicaciones clínicas y potencial diagnóstico
Uno de los aportes más relevantes es que amplía la forma de entender esta enfermedad. Tradicionalmente, el foco estuvo puesto en las mutaciones genéticas. Sin embargo, los resultados muestran que el contexto y la historia celular también resultan determinantes.
Factores como la alimentación, el estilo de vida o la exposición a ciertas sustancias pueden desencadenar procesos inflamatorios que dejan huellas duraderas en el organismo.
Este enfoque resulta especialmente importante en un escenario en el que los casos en personas jóvenes han aumentado en las últimas décadas. Según los investigadores, este fenómeno no puede explicarse únicamente por causas hereditarias, lo que refuerza el papel del ambiente y de los cambios recientes en los hábitos.

Uno de los aspectos más prometedores es su posible aplicación clínica. El equipo analiza si estas marcas pueden identificarse en muestras de heces, lo que permitiría detectar a personas con mayor probabilidad de desarrollar tumores.
Este tipo de herramientas facilitaría diagnósticos más tempranos y mejoraría el pronóstico, ya que permitiría intervenir antes de que aparezcan lesiones avanzadas. Además, abre la puerta al desarrollo de terapias dirigidas a revertir o reducir el impacto de estas alteraciones, lo que podría modificar el enfoque actual de tratamiento.
Perspectiva institucional y próximo paso en la investigación
El estudio forma parte de la iniciativa Cancer Grand Challenges, orientada a responder preguntas fundamentales sobre el origen de esta enfermedad. Si bien los resultados son prometedores, los investigadores señalan que aún deben confirmarse en humanos.
Por su parte, David Scott, director de la plataforma, destacó que el trabajo representa un avance significativo y podría orientar nuevas estrategias de prevención. El siguiente paso será trasladar estos hallazgos a ensayos clínicos, con el objetivo de evaluar su utilidad en pacientes y su posible implementación en la práctica médica.
Los resultados proponen una mirada más amplia sobre el origen de esta patología. Ya no se trata solo de mutaciones, sino también de la historia que acumulan las células a lo largo del tiempo.
En ese recorrido, la inflamación aparece como un factor capaz de dejar señales profundas y persistentes. Comprender este mecanismo no solo permite explicar mejor el origen del cáncer, sino que también abre nuevas oportunidades para prevenirlo.
Últimas Noticias
Por qué se pierde el apetito durante una infección: descubren una señal entre el intestino y el cerebro
La investigación, realizada en modelos animales, permite comprender cómo el organismo prioriza sus defensas al ajustar el consumo de alimentos frente a la presencia de párasitos

Nuevo hito del Garrahan: cómo fue el doble trasplante simultáneo que se realizó durante la madrugada
Más de 50 especialistas trabajaron para completar con éxito dos intervenciones inéditas en un nene de 7 años y un adolescente de 14. Jefes médicos contaron a Infobae los detalles
Testosterona y envejecimiento masculino: cómo afecta la salud integral y qué hacer ante su descenso
Valores insuficientes pueden reducir la motivación y alterar la concentración, mientras hábitos diarios y la actividad física contribuyen a preservar el bienestar integral

¿Repetir comidas ayuda a adelgazar? Qué reveló un estudio
Investigadores de Estados Unidos analizaron durante doce semanas los registros alimentarios y el peso diario de adultos con exceso de masa corporal. Cuáles fueron los resultados

¿Aprender o moverse? Cómo el cerebro puede decidir en milisegundos qué debe hacer
La nueva comprensión sobre la interacción exacta de dos señales químicas, obtenida en modelos animales, podría orientar la creación de tratamientos innovadores para trastornos cerebrales, como el Parkinson



