
Entre los principales genes que hace que uno de cada dos hombres y casi una de cada tres mujeres desarrollen cáncer a lo largo de su vida se encuentra el denominado KRAS, descubierto en 1982.
Desde hace más de 40 años, los científicos están intentando descubrir el talón de Aquiles de este gen, que es responsable de casi el 90% de los casos de cáncer de páncreas, el 40% de los de colon y el 35% de los de pulmón.
Ahora, un equipo del Centro de Regulación Genómica en Barcelona y del Instituto Wellcome Sanger en Cambridge (Reino Unido), ha identificado nuevos tratamientos terapéuticos de la proteína KRAS que pueden ser muy valiosos para el desarrollo de fármacos, ya que podría controlar los efectos de una de las causas más importantes del cáncer. El estudio, que presenta el primer mapa de control completo obtenido hasta ahora para cualquier proteína, fue publicado en la revista Nature.
KRAS es uno de los genes mutados con mayor frecuencia en muchos tipos de cáncer. Se encuentra en 1 de cada 10 cánceres humanos, con mayor prevalencia en tipos mortales como el cáncer de páncreas o de pulmón. Se la ha llamado la proteína “Estrella de la Muerte” debido a su forma esférica y a la falta de un buen sitio al que apuntar con los fármacos. Por esta razón, históricamente se ha considerado que KRAS es “no farmacológico” desde que se descubrió por primera vez en 1982.
En estas cuatro décadas, los científicos solo han podido avanzar en bloquear su sistema de comunicación alosteriano, que son señales moleculares que funcionan a través de un mecanismo de llave y cerradura por control remoto. Para controlar una proteína, se necesita una llave (un compuesto químico o fármaco) que pueda abrir una cerradura (sitio activo).
Las proteínas también pueden verse influenciadas por un bloqueo secundario (sitio alostérico) que se encuentra en otra parte de su superficie. Cuando una molécula se une a un sitio alostérico, provoca un cambio en la forma de la proteína, que puede alterar su actividad o su capacidad para unirse a otras moléculas, por ejemplo, cambiando la estructura interna de su cerradura principal.
En el desarrollo de nuevos fármacos, apuntar a los sitios alostéricos es clave, ya que ofrecen una mayor especificidad y reducen la probabilidad de efectos secundarios. También pueden cambiar la actividad de una proteína de manera más sutil, ofreciendo potencial para ajustar su función. Los fármacos que se dirigen a los sitios alostéricos son generalmente más seguros y eficaces en comparación con aquellos que se aplican directamente en sitios activos.
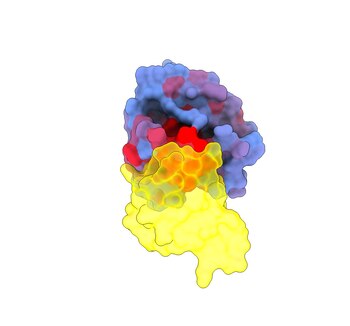
El gran problema es que estos sitios alostéricos son muy esquivos. A pesar de años de investigación, decenas de miles de publicaciones científicas y más de trescientas estructuras publicadas de KRAS, sólo dos fármacos han sido aprobados para uso clínico: sotorasib y adagrasib. Estos medicamentos actúan adhiriéndose a una bolsa adyacente al sitio activo, induciendo un cambio conformacional alostérico en la proteína que impide que se active.
“Nos llevó décadas producir un fármaco que funcionara contra KRAS, en parte porque carecíamos de herramientas para identificar sitios alostéricos a escala, lo que significaba que buscábamos sitios objetivo terapéuticos en la oscuridad. En este estudio demostramos un nuevo enfoque que puede mapear sistemáticamente sitios alostéricos para proteínas completas. A los efectos del descubrimiento de fármacos, es como encender las luces y dejar al descubierto las muchas formas en que podemos controlar una proteína”, explicó el doctor André Faure, científico del Centro de Regulación Genómica y coautor del estudio.
El doctor Darío Niewiadomski, médico oncólogo, miembro de la Sociedad Argentina de Cancerología, precisó a Infobae que “el ADN es una doble cadena de material genético, que está compuesto por muchísimos genes y algunos genes se llaman proto-oncogenes, y estos son, cuando están mutados, los que tienen alta posibilidad de desarrollar cáncer”.

“Para que se produzca el cáncer no es necesario que se activen una o dos mutaciones de genes. Tiene que haber varias mutaciones de ellos. Los genes más sensibles son los proto-oncogenes, que son los genes que pueden llegar a desarrollar cáncer. El KRAS es uno de estos genes y es bastante sensible. Según se estudió en muchos tumores, se trata de un gen que puede estar mutado o no. Cuando hay mutación del gen KRAS, significa que hay posibilidad de indicar cierta medicación al paciente y si no estuvieran mutado, esa medicación no se puede dar”, agregó el experto.
Y analizó: “Es por eso que la activación del gen KRAS, hace que la célula crezca de manera descontrolada. Por eso hay algunos tratamientos que se enfocan en este gen, lo bloquean, entonces hacen que esta célula no se siga dividiendo”.
Cuatro objetivos prometedores para fármacos más seguros y eficaces
Los autores del estudio mapearon los sitios alostéricos utilizando una técnica llamada escaneo mutacional profundo que implicó crear más de 26.000 variaciones de la proteína KRAS, cambiando sólo uno o dos componentes básicos (aminoácidos) a la vez.

Esto significó la primera vez que se consiguió realizar un mapa completo de los puntos débiles —o alostéricos— de una proteína, según destacaron los autores, encabezados por el biólogo británico Ben Lehner y su colega chino Chenchun Weng. Los investigadores subrayaron que hay miles de proteínas asociadas a cientos de enfermedades humanas, pero muy pocas han sido controladas con fármacos.
El equipo comprobó cómo estas diferentes variaciones de KRAS se unen a otras seis proteínas, incluidas aquellas críticas para que este gen impulse el desarrollo de tumores. Los investigadores utilizaron software de inteligencia artificial para analizar los datos, detectar alosteria e identificar la ubicación de sitios terapéuticos nuevos y conocidos.
“El único punto fuerte de nuestro método es su escalabilidad. Sólo en este trabajo realizamos más de 22.000 mediciones biofísicas, un número similar al total jamás realizado para todas las proteínas antes de que comenzáramos a aprovechar los notables avances en las metodologías de secuenciación y síntesis de ADN. Se trata de una enorme aceleración y demuestra el poder y el potencial del enfoque”, sostuvo Weng, primer autor del estudio e investigador postdoctoral en el Centro de Regulación Genómica.

“Nuestro estudio representa una nueva estrategia para atacar estas proteínas y acelerar el desarrollo de fármacos para controlar su actividad. La naturaleza de apuntar a sitios alostéricos significa que los medicamentos resultantes probablemente sean tratamientos más seguros y efectivos que los que tenemos ahora”, agregó el profesor de investigación ICREA, Ben Lehner, autor principal del estudio del Centro de Regulación Genómica y el Instituto Wellcome Sanger.
La técnica reveló que KRAS tiene muchos más sitios alostéricos fuertes de lo esperado. Las mutaciones en estos sitios inhibieron la unión de la proteína a sus tres socios principales, lo que sugiere que es posible inhibir ampliamente la actividad de KRAS.
Un subconjunto de estos sitios es particularmente interesante ya que están ubicados en cuatro bolsas diferentes de fácil acceso en la superficie de la proteína y representan objetivos prometedores para futuros fármacos. Los autores del estudio destacan uno en particular, el “bolsillo 3″, como particularmente interesante. Este bolsillo se encuentra lejos del sitio activo de KRAS y, por lo tanto, hasta ahora ha recibido muy poca atención por parte de las compañías farmacéuticas.

Los investigadores también descubrieron que pequeñas alteraciones en KRAS pueden cambiar drásticamente su comportamiento con sus socios, haciendo que la proteína prefiera una a otra. Esto tiene implicaciones importantes porque podría conducir a nuevas estrategias que controlen la actividad aberrante de KRAS sin obstaculizar su función normal en tejidos no cancerosos.
Ahorrar las versiones normales de KRAS significa menos efectos secundarios y tratamientos más seguros y eficaces. Los investigadores también podrían utilizar este conocimiento para profundizar en la biología de KRAS y explicar cómo se comporta la proteína en diversos escenarios, lo que podría ser clave para determinar su papel en diferentes tipos de cáncer.
“Las implicancias que tiene este estudio son fundamentalmente a raíz de los nuevos tratamientos que se podrían llegar a descubrir para poder neutralizar o desbloquear esta mutación genética y así poder tratar a distintos pacientes, a las distintas patologías. Si un tumor es resistente a ciertas drogas, quizá tener otras alternativas terapéuticas para poder tratar y seguir a los pacientes mejoraría la expectativa de vida y alargando la sobrevida global”, concluyó Niewiadomski.
Últimas Noticias
Hito en neurología: crearon neuronas humanas a partir de células de un paciente argentino con Alzheimer hereditario
Por primera vez, científicos argentinos desarrollaron un modelo neuronal a partir de células madre. Permitió observar cómo se desencadenan los daños en el cerebro y, a futuro, pensar en tratamientos a medida. Un antes y un después para la investigación del Alzheimer y otras neurodegenerativas
¿Qué es un embarazo ectópico, la emergencia médica que sufrió Camila Fernández, hija de Alejandro Fernández?
Riesgos como hemorragias internas o síntomas poco específicos convierten esta condición en un desafío médico urgente para mujeres en edad fértil

Cáncer de pulmón: un método con IA busca reducir la mortalidad a través de la detección temprana
Un programa aplicado en Alemania utiliza tecnología avanzada y criterios de selección precisos para diagnosticar la enfermedad en etapas iniciales. Cómo apuntan a ampliar las posibilidades de tratamiento para personas con alto riesgo

Identifican compuestos que podrían frenar la degeneración macular y evitar la ceguera
Un equipo del Institute of Molecular and Clinical Ophthalmology Basel logró hallar nuevas moléculas capaces de proteger células clave de la retina ante el paso del tiempo. Cómo este avance podría prevenir la pérdida de visión
Científicos logran monitorear cómo el cerebro elimina toxinas durante el sueño: los beneficios para la salud
Un equipo de la Universidad de Oulu, en Finlandia, desarrolló una tecnología que permite rastrear en minutos el movimiento de líquidos cerebrales durante el descanso nocturno





