
La tarde de este jueves 28 de diciembre, la Comisión Federal para la Protección contra Riesgos Sanitarios (Cofepris) difundió un comunicado de prensa en el cual alertó a la población sobre la venta de tres medicamentos enfocados en tratamientos oncológicos y los cuales ponen en riesgo la integridad de la población ya que los fármacos son falsos y además son vendidos de manera ilegal.
La misiva en cuestión hace énfasis en que derivado de una identificación oportuna por parte de la empresa Baxter es que se identificó la venta ilegal del medicamento Endoxan de 1 gramo cuyo compuesto principal es ciclofosfamida como uno de los involucrados en este evento.
De acuerdo con lo expuesto por Cofepris, se puede identificar este medicamento apócrifo tanto por el número de lote y la caducidad. Sobre el primero descrito, se hace referencia en que la dependencia no proporcionó tal número de lote para los fármacos que se venden en México sino que fue exclusivo para los que se ofertan en países centroamericanos, por lo que en caso de contar con uno en territorio nacional, es muy grande la probabilidad de que sea falso.
Otro de los medicamentos que están en la mira son Darzalex 100 mg/5ml el cual fue identificado por la empresa Janssen-Cilag y la cual alertó a la agencia reguladora para con ello advertir al resto de los consumidores. En ese sentido, se trata de los lotes DDP1255 destinado para el medicamento Darzalex 400 mg/20ml y los lotes EEF2466 y HHT5917 que se ubican en el fármaco Darzalex 100 mg/5ml. Los antes mencionados en caso de tenerlos son falsos.
“Cofepris informa que el lote MBS2H04 de Darzalex 400 mg/20ml, está destinado sólo para el mercado colombiano, mientras que el lote LHS2649 fue desviado de la cadena de suministro original”.
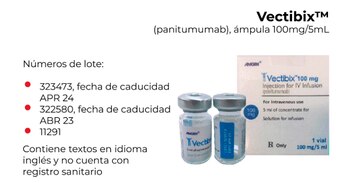
El último medicamento del cual se advierte a la población por ser falso, se trata de Vectibix 100mg/5mL el cual cuenta con textos en idioma inglés y a la vez cuentan con el número de lote 323473, caducidad abril 2024. Otros fármacos poseen en número de lote 322580 y 11291 con fecha límite abril 2023 de los que la dependencia ignora la importación que tuvo.
Con base a la información oficial, cada uno de los medicamentos antes descritos ponen en peligro la salud de quienes los consuman pues la dependencia no conoce las condiciones en las que fueron fabricados, al tiempo que tampoco se cuentan con datos en torno a su almacenamiento, por lo que la recomendación es suspender su uso y acudir ante un médico especializado y certificado para dar continuidad a los tratamientos adecuados para combatir la enfermedad.
Se pide identificar los productos
Aunque los productos antes mencionados fueron recientemente ubicados tanto por diversas empresas como por la Cofepris, la dependencia exhortó tanto a los consumidores como a los médicos a identificar de manera adecuada los productos antes descritos y, si se cuenta con más información que permita que no se ingieran o lleguen a manos de los pacientes, se dé aviso para poner en marcha la respectiva denuncia sanitaria a través de la plataforma gob.mx/Cofepris.
“Cofepris mantiene su compromiso de proteger la salud de todas y todos a través de acciones regulatorias y de control sanitario para prevenir que productos, empresas o establecimientos incumplan la legislación sanitaria vigente y representen un riesgo a la salud de la población”, remató la dependencia tras dar a conocer la información antes mencionada.
Más Noticias
Profepa reubica a 29 ejemplares de fauna silvestre tras operativo en Estado de México
Los animales fueron evaluados en su estado físico, de salud y condiciones de resguardo antes de ser trasladados

Temblor en México hoy: noticias de la actividad sísmica este sábado 28 de marzo de 2026
Sigue en vivo todas las actualizaciones sobre movimientos telúricos emitidas por el SSN

Arranca operativo de Semana Santa en CDMX con más de 10 mil policías
Las autoridades reforzarán la presencia policial en puntos de alta afluencia para prevenir la comisión de delitos

Melate, Revancha y Revanchita: números ganadores del sorteo de este 27 de marzo
El sorteo Melate se realiza tres veces a la semana, todos los miércoles, viernes y domingo, después de las 21:00 horas. Estos son los resultados del sorteo 4192 dados a conocer por la Lotería Nacional

Clima en Mazatlán: cuál será la temperatura máxima y mínima este 28 de marzo
Debido a su ubicación geográfica, que le dan una gran variedad de climas, México es uno de los países con mayor biodiversidad y es hogar de al menos 12% de las especies del mundo




