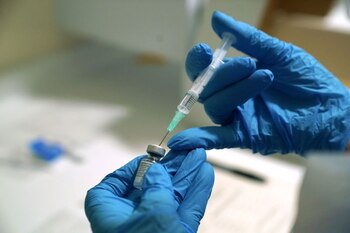
Nunca en la historia de la ciencia y la medicina se ha desarrollado una vacuna contra una enfermedad en forma tan acelerada. Tampoco nunca ha habido tantos científicos ni recursos dedicados a una sola enfermedad como ahora frente al SARS-CoV-2 que genera el COVID-19.
Hace un año en la ciudad de Wuhan, en China, surgió el nuevo coronavirus y desde el 10 de enero que científicos chinos publicaron el genoma del virus, cientos de laboratorios en todo el mundo comenzaron una carrera acelerada por desarrollar una vacuna eficaz que lo prevenga. Hasta ahora, el nuevo coronavirus ha infectado a 78 millones de persona y ha matado a más de 1,7 millones.
La carrera por la vacuna – que ya se compara con la carrera espacial – es uno de los espectáculos científicos más atrapantes que estamos viviendo día a día en esta crisis sanitaria mundial. Así, en los últimos diez meses hemos visto avances, acuerdos, efectos secundarios, aprobaciones, aplicaciones y también el incremento bursátil de los laboratorios que las desarrollan. También presenciamos los anuncios de compras millonarias, y algunas reticencias en la población para vacunarse y algunos pocos efectos adversos leves conocidos.

Las vacunas contra las enfermedades infecciosas han sido uno de los mayores éxitos en la historia de la humanidad, reduciendo efectivamente la carga de morbilidad de muchos patógenos. Incluso han permitido eliminar de la faz de la tierra un virus humano (viruela) y un virus del ganado (el de la peste bovina). “Esta no fue una carrera de candidatos a vacunas entre sí, sino una carrera contra el virus”, explicó Florian Krammer del Departamento de Microbiología de la Escuela de Medicina Icahn en Mount Sinai, Nueva York. El desarrollo de la vacuna SARS-CoV-2 avanza a una velocidad récord que no tiene precedentes, y es probable que las vacunas sean clave para resolver finalmente esta situación y salven millones de vidas. “Sin embargo, las vacunas se necesitaban mucho antes, lo antes posible”, explicó Krammer en un nuevo artículo de la revista Cell que pone en debate cómo asegurar que estén disponibles dentro del trimestre posterior a un nuevo brote.
Si bien es poco probable que hubieran evitado que el virus se globalizara, una infraestructura bien preparada capaz de producir vacunas entre 3 y 4 meses después del brote habría salvado muchas vidas y probablemente habría normalizado la situación en muchas áreas geográficas. Según los científicos, el desarrollo de una vacuna tradicional puede demorar 10, 15 años o más. El comienzo se inicia con una fase de descubrimiento prolongada en el tiempo que implica el diseño y realización de experimentos exploratorios. Luego, se realizan experimentos preclínicos y estudios de toxicología, así como el desarrollo de procesos de producción. Durante este proceso, se presenta una solicitud de investigación de nuevo fármaco (IND) y se comienzan de forma secuencial los ensayos de fase I, II y III.

Después de completar los ensayos de fase III, y luego de cumplidos los puntos finales predeterminados (end points), se presenta una solicitud de licencia biológica (BLA, del inglés biologics license application) que es revisada por las agencias reguladoras y finalmente se autoriza. Después de ese punto comienza la producción a gran escala. Tanto la vacuna contra la varicela como FluMist, que protege contra varias cepas del virus de la influenza, tardaron 28 años en desarrollarse. Se necesitaron 15 años para desarrollar una vacuna contra el virus del papiloma humano, que puede causar seis tipos de cáncer. También se necesitaron 15 años para desarrollar una vacuna contra el rotavirus, que comúnmente causa diarrea acuosa grave. Jonas Salk tardó seis años en desarrollar y probar la primera vacuna contra la polio, comenzando con el aislamiento del virus.
Hasta ahora, la inmunización que se había conseguido en menos tiempo fue la del ébola, lograda en cinco años. Pero la pandemia, con todo lo que trajo aparejado, ha obligado a pisar el acelerador a fin de acortar los tiempos, sin eliminar los pasos que aseguren la eficacia, la calidad y la seguridad.

Tal y como vemos en la figura, el desarrollo de vacunas para el SARS-CoV-2 ha seguido un proceso temporal acelerado por distintos motivos:
– Debido a los conocimientos adquiridos previos en el desarrollo inicial de las vacunas para el SARS-CoV y el MERS-CoV, se omitió la fase de descubrimiento.
– Se adaptaron los procesos existentes y se iniciaron los ensayos de fase I / II casi de forma simultánea.
– Los ensayos de fase III se iniciaron después del análisis intermedio de los resultados de las fases anteriores, manteniendo etapas de ensayos clínicos en paralelo.
– Mientras tanto se comenzó la producción a gran escala (a riesgo) de varias vacunas.
– La Agencia Europea del Medicamento, EMA, ha realizado una evaluación continua de estas vacunas.

¿Cómo se desarrolló esta vacuna tan rápidamente? Las vacunas de ARNm producidas por Pfizer y Moderna son más rápidas de desarrollar, ya que no requieren que las empresas produzcan proteínas o patógenos debilitados para la vacuna. Las vacunas tradicionales generalmente usan una versión debilitada del patógeno o una porción de proteína, pero debido a que estos se cultivan en huevos o células, desarrollar y fabricar vacunas lleva mucho tiempo.
Por el contrario, al usar solo el material genético que produce la glicoproteína Spike, la proteína en la superficie del coronavirus que es esencial para infectar las células humanas, se simplifica el diseño y la fabricación de la vacuna. El ARNm de material genético es fácil de hacer en un laboratorio. La fabricación de una vacuna de ARNm en lugar de una vacuna proteica puede ahorrar meses, sino años. Otro factor que aceleró el desarrollo de vacunas fue el reclutamiento rápido y eficiente de pacientes para ensayos clínicos.
¿Cómo se garantiza la seguridad cuando el desarrollo de vacunas es tan rápido? La seguridad es el principal objetivo de una vacuna. La razón por la que las vacunas pueden aprobarse tan rápidamente es que los grandes ensayos clínicos para evaluar la eficacia y seguridad de las vacunas se están realizando al mismo tiempo que la preparación de fabricación a gran escala, financiada por el programa Operation Warp Speed del gobierno federal. Por lo general, la fabricación a gran escala comienza solo una vez que la vacuna se ha probado en ensayos clínicos.

En el caso del COVID-19, el gobierno de los EE.UU. quería estar listo para comenzar a distribuir la vacuna en el momento en que se conocieran los resultados de los ensayos de fase 3 y se analizaran los datos de seguridad. Con este fin, las compañías farmacéuticas lanzaron la fabricación en riesgo, lo que significa que las dosis de vacuna fabricadas se desecharían si no fuera ineficaz o insegura, durante el período de espera de seguridad de dos meses exigido por la FDA. La ventaja es que si la vacuna es segura y eficaz, se puede distribuir de inmediato y puede comenzar la vacunación.
¿Son estas vacunas más riesgosas que otras? No se han aprobado vacunas de ARNm antes porque es una tecnología relativamente nueva. Pero estas vacunas de ARNm parecen seguras y no presentan mayor riesgo que otras que ya han sido probadas, como la vacuna infantil contra el sarampión. Hasta la fecha, no se han reportado efectos secundarios significativos en los estudios intermedios de fase 3 de las vacunas Moderna y Pfizer.

Los efectos secundarios que se han informado son cosas menores que uno esperaría con cualquier vacuna, incluido dolor en el lugar de la inyección y fatiga transitoria, dolores musculares o articulares. La FDA exige que una vacuna COVID-19 sea al menos 50% efectiva para prevenir enfermedades sintomáticas. También requiere una mediana de dos meses de seguimiento después de completar la vacunación para la mitad de los receptores de la vacuna (para la mayoría de las vacunas son dos dosis). Este período de dos meses es para permitir la detección de un evento adverso de la vacuna.
Pero los expertos coinciden en que el éxito de tener una vacuna en pocos meses fue gracias a una inversión sin precedentes, en muchos casos a riesgo, más el conocimiento científico de miles de laboratorios del mundo trabajando al mismo tiempo y una red de colaboración sin igual. Los Estados han invertido grandes cantidades de dinero. Y el proyecto Covax en la Organización Mundial de la Salud (OMS) o el WRAP en Estados Unidos han sido fundamentales para permitir que las empresas, sobre todo algunas más pequeñas como Moderna, entraran en esta carrera.
Laboratorios como Pfizer o AstraZeneca, ensayaban la vacuna mientras las estaba produciendo y empaquetando. Con el riesgo de que si esta vacuna nunca sale, millones de dosis se perderían.
SEGUÍ LEYENDO:
Últimas Noticias
Los nuevos 60: los cambios en la dieta adulta que pueden agregar casi 10 años de vida
Los cambios en la dieta en la edad adulta pueden agregar casi 10 años de vida según un amplio estudio científico. Una guía de pequeños grandes hábitos para alcanzar la plenitud

9 tips para comenzar a hacer deporte y mejorar el estado físico
Una guía para evitar las excusas y ponerse en movimiento. Incorporar desafíos de manera paulatina y armar una rutina son los pasos claves para empezar

Día Mundial del Pene: cuidados para la higiene adecuada y consejos para prevenir el cáncer y otras enfermedades
La fecha busca celebrar la fertilidad y generar conciencia acerca de la práctica del sexo seguro. La salud y el cuidado del órgano reproductor masculino son fundamentales para mantener una vida sexual plena y saludable

Turbulencias durante el vuelo: cinco consejos para subirse al avión sin miedo
Un piloto comercial explica por qué son habituales estos movimientos, además brindó recomendaciones sobre qué asiento elegir para sufrir menos durante el viaje. Una guía práctica y sencilla sobre algunos de los puntos más consultados por los pasajeros

Cuáles son los tres desayunos ideales para personas con diabetes e hipertensión
Las clásicas tostadas con mermelada pueden reemplazarse por opciones más saludables, con más proteínas, fibras y minerales. Cómo ayudan a controlar estas enfermedades



