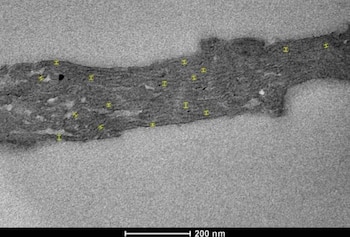
Por primera vez, científicos han logrado lo que antes parecía una contradicción biológica: células animales capaces de realizar la fotosíntesis. Este avance, desarrollado en el Laboratorio de Biología Integrada de la Universidad de Tokio y publicado en J-STAGE, la plataforma que recopila investigaciones académicos japoneses, representa un cambio significativo en el campo de la biología y plantea aplicaciones potenciales en medicina y producción de alimentos. El equipo, dirigido por el profesor Sachihiro Matsunaga, ha conseguido integrar cloroplastos activos en células de mamíferos, logrando reacciones fotosintéticas similares a las de plantas y algas.
La fotosíntesis es un proceso bioquímico mediante el cual plantas, algas y algunas bacterias transforman la luz solar en energía química. Este fenómeno, fundamental para la vida en la Tierra, utiliza cloroplastos —orgánulos especializados en las células vegetales— para convertir la luz, agua y dióxido de carbono en oxígeno y glucosa, fuente de alimento para las plantas. En cambio, los organismos animales, incluidos los seres humanos, se sustentan a partir del consumo de oxígeno y la descomposición de los alimentos.
Durante años, el hecho de que la fotosíntesis estuviera limitada a organismos con cloroplastos parecía una barrera insuperable en biología. Desde la década de 1970, diversos científicos intentaron introducir esta capacidad en células animales, pero se encontraron con obstáculos importantes. Los cloroplastos, al ser reconocidos como material extraño, eran destruidos rápidamente por las células animales, lo que impidió obtener resultados estables. Adicionalmente, la mayoría de los cloroplastos funcionan a temperaturas de hasta 30°C, mientras que las células de mamíferos suelen cultivarse a 37°C, una diferencia que inhibía su actividad fotosintética en entornos celulares de animales.
Cloroplastos resistentes al calor: Un avance clave
Para superar estas barreras, el equipo de Matsunaga buscó cloroplastos que pudieran soportar temperaturas similares a las del cuerpo humano. Después de años de investigación, hallaron una solución en Cyanidioschyzon merolae, una alga roja primitiva que sobrevive en ambientes extremos como fuentes termales volcánicas a 42°C. Estas condiciones de vida extremas le permiten a esta alga realizar la fotosíntesis a temperaturas superiores a las de la mayoría de las plantas y algas comunes. Los cloroplastos aislados de Cyanidioschyzon merolae demostraron así una capacidad única para funcionar en las células de animales, superando una de las principales barreras de este tipo de investigación.
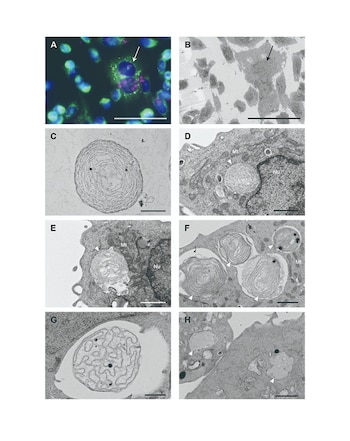
El equipo extrajo y purificó los cloroplastos de esta alga, introduciéndolos en células de mamíferos, específicamente en células de ovario de hámster (CHO-K1), una línea celular comúnmente utilizada en investigación por su facilidad para aceptar materiales externos. Una vez en las células animales, estos cloroplastos pudieron mantener su estructura y mostrar actividad fotosintética durante al menos dos días.
Otro de los obstáculos fue el rechazo de los cloroplastos por las células animales. Para superar esto, el equipo utilizó un enfoque novedoso: en lugar de forzar la entrada de los cloroplastos en las células animales, optaron por introducirlos como “alimento”. Esto permitió que los cloroplastos fueran ingeridos por las células y evitaran la rápida destrucción que había sido el problema en investigaciones previas. Este enfoque permitió que, al menos temporalmente, las células animales mantuvieran los cloroplastos activos en su interior sin activarse los mecanismos de degradación celular.
“Con esta técnica, los cloroplastos ingeridos como alimento se mantuvieron en las células animales durante aproximadamente dos días, y logramos detectar las primeras reacciones de fotosíntesis en un entorno animal”, explicó Matsunaga a Newsweek. Esta estrategia logró algo que los investigadores consideraban imposible hace apenas unos años y ha permitido que los cloroplastos produzcan oxígeno y proporcionen una fuente adicional de alimento para la célula animal huésped.
Implicaciones para la medicina y la investigación alimentaria
El desarrollo de células animales con capacidad de fotosíntesis abre un mundo de posibilidades en biomedicina y biotecnología. Uno de los usos potenciales que el equipo de investigación visualiza es la creación de mini órganos artificiales para estudiar enfermedades y probar nuevos tratamientos. La falta de oxígeno en el interior de cultivos celulares de múltiples capas es un problema frecuente en la investigación médica, pues limita la capacidad de los tejidos artificiales para crecer y desarrollarse. Al dotar de cloroplastos a estas células, sería posible suministrar oxígeno directamente al interior de las estructuras celulares iluminadas, promoviendo así el crecimiento y la longevidad de estos tejidos.
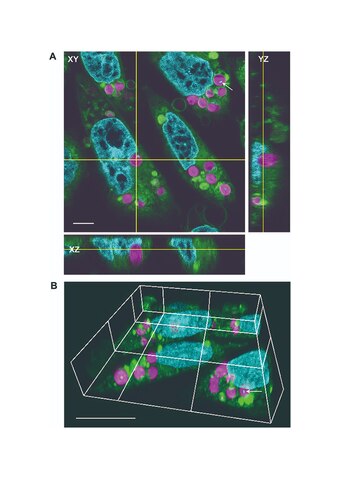
Otra posible aplicación es en la producción de carne cultivada en laboratorio. Uno de los principales desafíos en este sector es lograr que las células animales crezcan en grandes cantidades sin requerir continuamente nutrientes externos. La fotosíntesis en células animales podría reducir la dependencia de nutrientes externos al proporcionar energía adicional directamente a las células de carne cultivada, haciéndola potencialmente más sostenible y económica.
Limitaciones y pasos futuros
Aunque el avance es significativo, la tecnología está lejos de estar lista para aplicaciones clínicas o comerciales. Actualmente, los cloroplastos pueden realizar fotosíntesis en células animales durante un máximo de dos días antes de ser degradados o volverse inactivos. “En el futuro, queremos mejorar esta técnica para que los cloroplastos puedan llevar a cabo fotosíntesis en células animales durante el mayor tiempo posible”, afirmó Matsunaga. La capacidad de mantener los cloroplastos activos a largo plazo es una prioridad para futuras investigaciones, y podrían necesitarse modificaciones genéticas en las células huésped para mejorar la integración y compatibilidad.
Un campo de estudio potencial para prolongar la viabilidad de los cloroplastos es la observación de organismos que ya realizan fotosíntesis de forma simbiotica, como algunos moluscos marinos y salamandras. Estos organismos han desarrollado adaptaciones para mantener las algas en su organismo durante períodos prolongados sin que sean destruidas, un mecanismo que podría replicarse en futuras investigaciones.
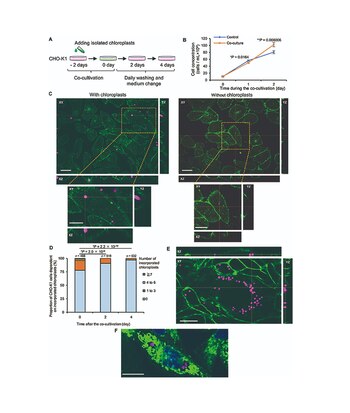
El logro del equipo de Matsunaga marca un paso importante en el campo de la biología sintética, un área que busca replicar o modificar funciones biológicas en organismos vivos. Con esta investigación, se abre la posibilidad de desarrollar nuevos tratamientos médicos y mejorar la eficiencia de la producción de alimentos en laboratorio, demostrando que el límite entre el mundo animal y vegetal puede ser más flexible de lo que se pensaba.
Este avance también plantea preguntas sobre las capacidades de adaptación de las células animales y sobre cómo los conocimientos de la fotosíntesis en células de mamíferos podrían cambiar el futuro de la ciencia y la medicina.
Últimas Noticias
Descubren cómo cuatro bacterias intestinales pueden transformar la grasa corporal y el metabolismo
A partir de experimentos en ratones, científicos detectaron que una red de bacterias traduce la comida en señales que activan el metabolismo de formas insospechadas. Por qué los resultados pueden ser claves para la prevención de la obesidad

Los astronautas de Artemis II rompieron el primer récord mundial en órbita a la Tierra
Volaron a más de 70.000 kilómetros alrededor de nuestro planeta antes de comenzar el nuevo encendido de motores que los ubicará en trayectoria lunar
El brazo secreto del pulpo macho: la evolución que asegura la reproducción
Investigadores identificaron que una sola extremidad, el hectocótilo, se especializa en transferir espermatóforos durante el apareamiento y es protegida de forma activa por el animal, revelando una estrategia única entre los cefalópodos

Cómo un hallazgo en salmones podría cambiar la forma de entender la salud de los océanos
El trabajo de investigación utiliza conservas almacenadas por décadas para aportar datos inesperados sobre la reconstrucción de cadenas alimentarias y la influencia de políticas ambientales en especies emblemáticas del norte del Pacífico

Misión Artemis II de la NASA: los astronautas realizaron una maniobra clave de altura de la nave espacial
En el inicio de la segunda jornada histórica de la exploración espacial hacia la Luna la tripulación rompió un nuevo récord orbital. Todos los detalles





