La vacuna bivalente argentina contra el COVID-19 “ARVAC Cecilia Grierson” comienza a transitar la fase final de los ensayos clínicos. El objetivo es que la reguladora local ANMAT apruebe esta fórmula durante 2023. Tal como adelantó Infobae, el 6 de febrero fue el momento en el que esta etapa comenzó. Ahora, el Ministro de Ciencia y Tecnología, Daniel Filmus, mantuvo un encuentro con el equipo liderado por la investigadora Juliana Cassataro para conocer los últimos avances.
Es que esta inmunización ya se evaluó en 100 voluntarios, de entre 18 y 60 años, y en las próximas semanas se abrirá la inscripción para avanzar con una segunda etapa en 10 centros de todo el país. “Es el resultado de la enorme tarea realizada por nuestras científicas y científicos y del trabajo conjunto entre el Ministerio de Ciencia, el Ministerio de Salud, el CONICET, la UNSAM y el Laboratorio Cassará”, señaló Filmus durante su presencia en la Universidad Nacional de San Martín.
“Esta vacuna es un motivo de orgullo para la Argentina y significa un ejemplo virtuoso de articulación público-privada”, agregó el ministro, quien fue acompañado por el Presidente de la Agencia I+D+i, Fernando Peirano. Vale destacar que esta fase contó con un financiamiento de 1.100 millones de pesos por parte de la Agencia I+D+i, dependiente del MINCyT.
Esta inmunización, siguiendo con las recomendaciones de especialistas y de agencias de salud locales e internacionales, comenzará además la evaluación de una nueva versión bivalente de la fórmula, con un antígeno de Ómicron BA.4 y BA.5. Y según adelantaron a Infobae desde el laboratorio Pablo Cassará, ya cuentan con la capacidad industrial para producir hasta 5 millones de dosis mensuales de antígeno vacunal, y tienen proyectado comenzar su fabricación en paralelo al desarrollo de los mencionados estudios de Fase II/III.

“Estamos realmente muy felices de poder comenzar este ensayo. La ARVAC Cecilia Grierson es la primera vacuna argentina en alcanzar las fases 2 y 3 de evaluación. En esta etapa, 100 voluntarias y voluntarios de entre 18 y 60 años ya fueron inoculados y, próximamente, se abrirá la inscripción para avanzar con una segunda etapa en 10 centros de todo el país que contempla ensayos en 1.800 personas mayores de 18 años, en algunos casos, con comorbilidades”, detalló Cassataro, bióloga (UNSAM), doctora en Inmunología y líder del equipo UNSAM-CONICET que trabaja en esta vacuna. Mientras el estudio de Fase II/III cuenta con la incorporación y el aporte del grupo de trabajo del doctor e investigador Gonzalo Pérez Marc.
Cronología de un avance argentino
Este proyecto es el resultado del esfuerzo coordinado de más de 200 personas de distintas disciplinas, pertenecientes a más de 20 instituciones públicas y privadas y a otros 12 sitios de investigación clínica. “Durante la pandemia, Argentina tuvo que esperar a que los productores de vacunas abastecieran a los países en los que estaban instalados. Tener una plataforma propia para la región es muy importante para que eso no vuelva a ocurrir, en caso de que haya una nueva pandemia o que las variantes que circulen en nuestra región no sean las mismas que en el norte”, había resaltado la experta en diálogo con Infobae.
Tras alcanzar resultados positivos en la Fase I, en los primeros días del 2023 la Administración Nacional de Medicamentos, Alimentos y Tecnología Médica (ANMAT) autorizó el inicio de los estudios de Fase II/III. En este punto, los expertos buscan evaluar la seguridad, tolerabilidad e inmunogenicidad del inoculante; siendo que la ARVAC es una vacuna proteica producida por biotecnología, una plataforma tecnológica muy segura que se utiliza desde hace décadas en inoculaciones para niños recién nacidos y adolescentes. De hecho, Cassará desarrolló y lanzó al mercado en 1997 la primera vacuna contra la Hepatitis B producida en la región.

“Este tipo de tecnología (producto basado en proteínas recombinantes) se guarda en la heladera (2 – 8 °C) y puede durar un año; por lo tanto, para la distribución en lugares remotos donde no tienen acceso a un freezer de -70 es sustancial. Y otro tema es que esta plataforma ya tiene la capacidad de manufactura en la región. Ya hay plantas que producen anticuerpos monoclonales y pueden hacerlas a lo largo y ancho del país”, había señalado a Infobae otro de los científicos a cargo del desarrollo, Juan Manuel Rodríguez, quien es biólogo (UBA), y coordinador del área de I+D de biofármacos del Laboratorio y Fundación Pablo Cassará.
Durante el proceso tecnológico a escala industrial de ARVAC, que comenzó en el año 2021, se desarrollaron 5 tecnologías de producción de antígeno en las variantes del SARS-CoV-2 Wuhan, Gamma, Delta, Omicron B1 y Omicron BA.4 y BA.5. En el estudio de Fase I se comprobó que la fórmula es segura y que incrementa hasta 30 veces los anticuerpos neutralizantes contra Wuhan, Gamma y Ómicron. ARVAC está diseñada como vacuna de refuerzo, se puede almacenar y transportar refrigerada entre 2°C y 8 °C y, además, puede actualizarse su principio activo para hacer frente a nuevos sublinajes del virus que escapen a la respuesta inmunológica.
Un logro vital de la ciencia argentina
El camino de esta vacuna dio sus primeros pasos con el financiamiento inicial de la Agencia Nacional de Promoción de la Investigación, el Desarrollo Tecnológico y la Innovación (Agencia I+D+i) del Ministerio de Ciencia y Tecnología de la Nación. El siguiente, fue la inversión del Laboratorio Cassará en el desarrollo tecnológico y en los estudios de Fase I. 4. Es la primera vez que una vacuna contra enfermedades infecciosas diseñada y desarrollada integralmente en Argentina logra completar los estudios clínicos de Fase I.

“Este es un proyecto que enfoca la capacidad científico-tecnológica argentina en resolver necesidades concretas con alto impacto sanitario y económico. El proyecto va a dejar instalada una plataforma de desarrollo y producción de vacunas recombinantes que podrá ser utilizado para nuevas vacunas en el futuro”, destacó a este medio Jorge Cassará, directivo del laboratorio homónimo.
Vale recordar que, en esta segunda etapa de la Fase II/III, la vacuna será inoculada a unos 1800 voluntarios para que, durante 2023, la ANMAT apruebe su inoculación. Según habían detallado desde el Ministerio de Salud nacional, que lidera Carla Vizzotti, los estudios se realizarán “en voluntarios adultos previamente vacunados contra el virus SARS-CoV-2″
Seguir leyendo:
Últimas Noticias
Lanzamiento de la misión Artemis II a la Luna, en vivo: los astronautas ya se encuentran dentro de la nave espacial
Cuatro astronautas partirán hoy en un viaje de 10 días para orbitar nuestro satélite natural. Todos los detalles de la histórica misión espacial

El riesgo oculto de los plásticos: se asocian con más partos prematuros y pueden afectar la salud del bebé antes de nacer
Científicos de los Estados Unidos encontraron que compuestos químicos presentes en envases y juguetes están detrás de millones de nacimientos antes de término. Cómo se debería reducir la exposición durante el embarazo

El primer mapa genético completo del páncreas revela claves ocultas de la diabetes tipo 1
La tecnología utilizada en el estudio facilita intervenciones a medida al mostrar cómo evolucionan los mecanismos biológicos desde etapas asintomáticas hasta el desarrollo pleno de la patología

Qué es el propofol, el fármaco detrás de “los viajes controlados” vinculados a la muerte de un médico residente
La droga está en el centro de la escena tras la muerte de un joven médico por una sobredosis. Se trata de un anestésico intravenoso de acción ultrarrápida. Especialistas consultados por Infobae indicaron que sólo debe ser administrado bajo control profesional. Los graves riesgos que implica fuera del entorno médico

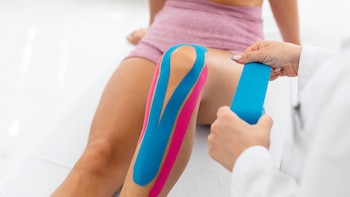
¿Las cintas de colores sirven para tratar el dolor muscular?: qué revela la evidencia científica reciente
Una investigación que revisó más de 3.000 estudios clínicos mostró que este producto usado por deportistas ofrece mejoría pasajera, sin demostrar un impacto sostenido sobre la recuperación ni la movilidad