La apuesta de estas tres vacunas contra el COVID-19 -Pfizer-Biontech (EEUU-Alemania), Moderna (EEUU) y Sputnik V (Rusia)- continúa con su incansable carrera de obstáculos, a pesar de las aprobaciones recibidas de las distintas agencias y organismos de regulación. Hasta hoy, el sello aprobatorio ocurrió bajo el contexto y uso de emergencia, tal como lo establece la actual pandemia global por el virus SARS-COV-2.
Elaborado por dos prestigiosas científicas argentinas, ellas son Mirna Biglione, médica especialista en Alergia e Inmunología del Instituto de Investigaciones Biomédicas en Retrovirus y Sida (INBIRS UBA-CONICET) desde Buenos Aires, Argentina; y Laura Bover, doctora en Biología Celular, Oncología, y Química Biológica de la UBA, desde la Universidad de Texas, Estados Unidos. Las científicas y sus equipos recopilaron datos obtenidos hasta el 1 de enero de 2021 y compararon su eficacia, componentes y contraindicaciones.
En diálogo exclusivo con Infobae desde Texas, la doctora en Biología Celular Laura Bover explicó: “Los datos que relevamos los obtuvimos de las referencias que figuran al pie de la tabla, analizando documentos y sitios web de la Administración de Medicamentos y Alimentos de los Estados Unidos (FDA), del Centro para el Control y Prevención de Enfermedades de EE. UU. (CDC), de un documento llamado “Lineamientos” publicado por el Ministerio de Salud de Argentina e información que presenta el sitio web de Gamaleya para Sputnik V”.
“En el sitio web de la FDA no tienen trabajos científicos de Sputnik en Fase III. Sólo hay una nota de Reuters y esos mismos datos son los que publica la cartera sanitaria local y el gobierno argentino”, alertó Bover, aunque apuntó que “afirman desde Gamaleya que próximamente los compartirán”.
De acuerdo a Bover, quien es actualmente directora del laboratorio de Anticuerpos Monoclonales del M.D. Anderson Cancer Center, el hospital número uno en el mundo para tratamientos contra el cáncer y lidera un grupo internacional de 60 científicos e investigadores que estudia la utilización del plasma de pacientes recuperados de COVID-19 como forma de tratamiento, “los porcentajes presentados se muestran así, como porcentajes pero no están los datos demográficos de los participantes en el estudio. Como si aparecen en las publicaciones de The New England Journal of Medicine (NEJM), la revista científica de alto impacto donde se publicaron los Fase III de Pfizer-Biontech y de Moderna. También allí se publicaron los datos del estudio clínico sobre plasma del Hospital Italiano. Gamaleya se supone que está preparando un estudio similar”.
“Las diferencias también las vimos en las autorizaciones de uso de emergencia, realizadas para Moderna y Pfizer por FDA en USA y algunos otros países. Sputnik fue aprobada tempranamente en Rusia y autorizada para uso de emergencia en Argentina”, añadió.
Consultada por Infobae, Mirna Biglione, desde Buenos Aires, y médica especialista en Alergia e Inmunología, del Instituto de Investigaciones Biomédicas en Retrovirus y SIDA (INBIRS) UBA-CONICET, explicó en referencia a la dificultad de compilar los datos oficiales y científicos de las vacunas: “cuando los datos de Fase III están publicados en revistas internacionales de referencia como lo es en este caso el NEJM, uno cuenta con datos fidedignos. Por el momento se cuenta con una publicación para la vacuna Sputnik V en una revista internacional pero de Fase I y II, faltarían los de Fase III. Hay que considerar otra situación, que los datos muestran que los participantes tanto en el caso de Moderna como de Pfizer son más respecto a los que formaron parte de Sputnik V”.
“En la Argentina contamos con los documentos que brinda el Ministerio de Salud, y en la página del Centro Gamaleya hay información que brinda Reuters, pero no contamos con datos tan exhaustivos en el caso de Sputnik V como sucede con Moderna/NIH y Pfizer/BioNTech, seguramente próximamente los publicarán”, añadió a Infobae.
Para la investigadora del INBIRS, no debemos olvidarnos que estamos ante una pandemia, las personas están cansadas. Ya son muchos días, vivimos cuarentenas y en algunos casos cuesta tomar conciencia en lo que respecta a los hábitos de protección individual: cómo usar de manera correcta el barbijo cuando uno no ve al virus. “Nuestro enemigo es invisible y la mayoría de las personas que se infectaron cuentan que tuvieron síntomas leves y eso no ayuda para que se tome conciencia de la importancia de lo que implica la enfermedad, especialmente para los médicos, enfermeros, ambulancieros, camilleros; aquellos que están viendo la otra cara de la moneda, la realidad del contacto con pacientes en terapia intensiva, moderados, graves o severos que siguen falleciendo en todo el mundo y aquí en la Argentina también”, aseveró Biglione.
“Estamos viviendo una situación nuevamente complicada y difícil en la Argentina, y por ello en este contexto debemos considerar que el avance científico que hubo con el desarrollo de vacunas más avanzadas que están dando una eficacia mayor al 90% es un gran logro y es la herramienta que tendremos a mano, pero que recién estamos comenzando a utilizar”, analizó.
De acuerdo a la investigadora del INBIRS “No estamos aún vacunados, el virus está entre nosotros, cada vez hay más casos; por eso, el cuidado y la prevención son más clave que nunca: hay que hacer hincapié en preservar a los grupos de riesgo, mayores de edad, personas con comorbilidades como diabetes, obesidad, enfermedad cardíaca, pulmonar crónica, inmunodeficiencia, trasplantados, entre otras”.
Las investigadoras Bover-Biglione compararon los puntos más importantes de estos inoculantes, como la eficacia, tipo de tecnología aplicada, componentes, advertencias y reacciones adversas/limitaciones de cada plataforma. Aquí un detalle de la información de los cuadros:
Tras la información veraz
El primer ítem al que se refirieron fue la eficacia general en la prevención de infección sintomática, a partir de los datos obtenidos del análisis de los estudios de Fase III en curso. La vacuna de Moderna, que cuenta con una autorización de la Unión Europea (UE), de la Administración de Medicamentos y Alimentos de los Estados Unidos (FDA) a partir de la publicación científica basada en los resultados parciales de Fase III multicéntrico en varios países del mundo al igual que la de Pfizer, mostró una eficacia del 94,1%, con 30.420 participantes, 8 semanas de seguimiento y aprobación al finalizar la Fase III. Cabe señalar que hasta ahora la vacuna del laboratorio de Moderna -en Massachusetts- solo prevé su fabricación para el territorio de los Estados Unidos.
Por su parte, la vacuna de Pfizer-BioNTech registró una eficacia de 95%, con 43.448 participantes, 8 semanas de seguimiento y aprobación definitiva al culminar la Fase III.
En el caso de la vacuna rusa Sputnik V, fue de 91,4%, con 22.714 personas en el ensayo, 3 semanas de seguimiento. Este inoculante fue aprobado en Rusia. “En nuestro país, la vacuna Sputnik se ha aprobado con el acceso a datos de Fase III que aún no han sido publicados en revistas cientificas”, mencionaron ambas investigadoras, que confeccionaron los cuadros comparativos para el INBIRS.
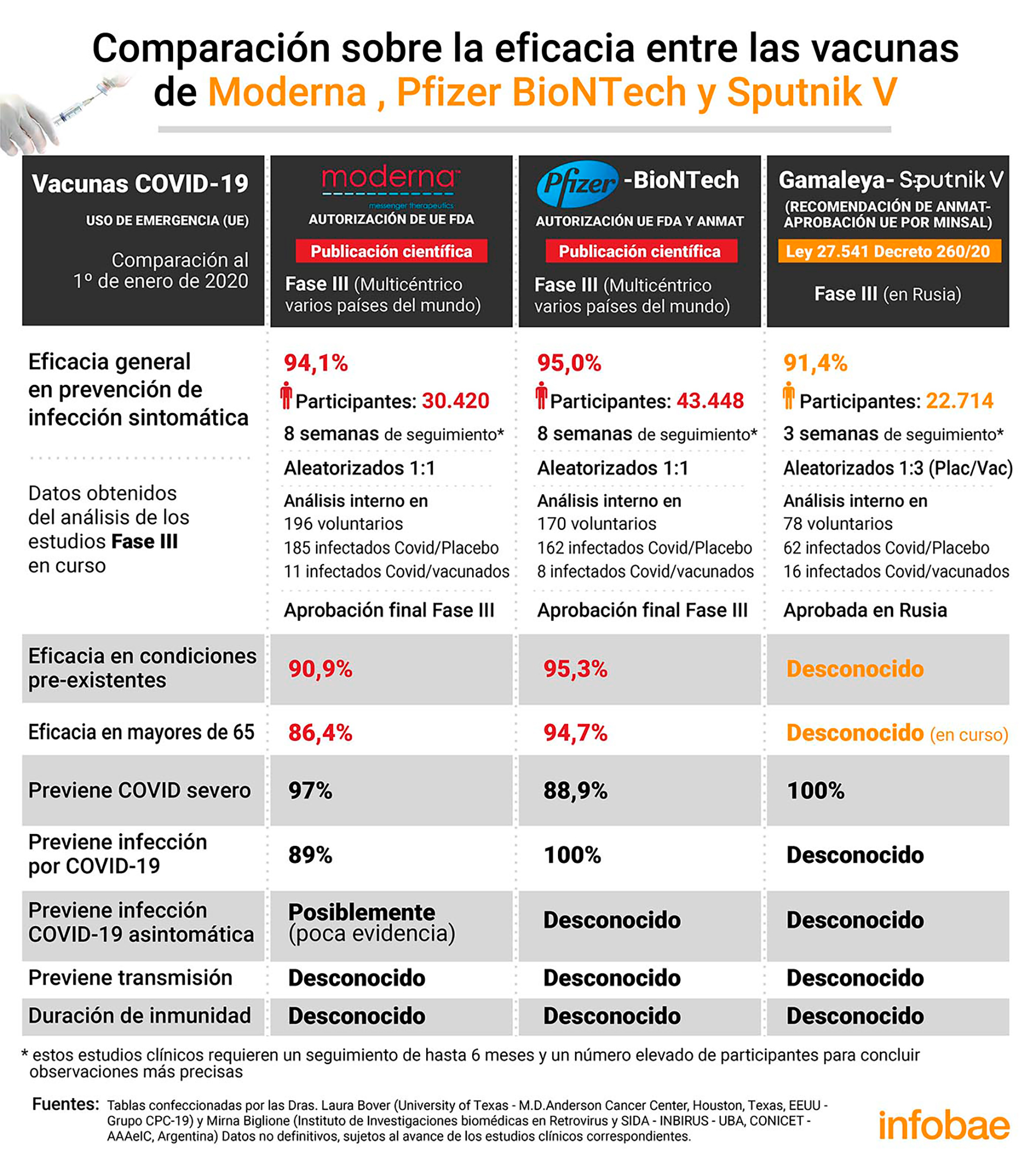
En la eficacia en condiciones preexistentes Moderna informó tener 90,9%, Pfizer 95,3% y en el caso de la vacuna de Gamaleya el dato es desconocido hasta el momento; en mayores de 65 años 86,4%, 94,7% y desconocido (en curso) respectivamente. En relación a la prevención del COVID-19 severo, la de Moderna mostró una efectividad del 97%, Pfizer 88,9% y Sputnik V 100%.
En el caso de las hospitalizaciones por el nuevo coronavirus, la vacuna de Moderna mostró un 89%, 100% de efectividad en el caso de Pfizer y desconocido en la de Gamaleya. ¿Estas 3 vacunas previenen la infección asintomática? En Moderna, posiblemente, aunque hay poca evidencia, y es un dato desconocido para la de Pfizer y Sputnik V. Tanto en la prevención de la transmisión como en la duración de la inmunidad la información en las 3 es desconocida. “Estos estudios clínicos requieren un seguimiento de hasta d y un número elevado de participantes para concluir observaciones más precisas”, advirtieron las investigadoras.
De acuerdo a lo manifestado a Infobae por Biglione, “existen más datos al día de hoy para las vacunas que publicaron sus resultados de Fase III en NEJM, Pfizer y Moderna, para los efectos adversos, más poblaciones estudiadas, una mayor cantidad de voluntarios incluidos que para la vacuna Sputnik V” y agregó: “Vamos a tener que esperar un tiempo para ver cómo evolucionan los resultados de estos ensayos de Fase III en el caso de todas las vacunas, ya que cabe destacar que están aprobadas para uso de emergencia”.
“Desde el Centro Gamaleya no mostraron aún pruebas suficientes, pero probablemente las tengan. No obstante la OMS sugiere que para que sea valedera una evaluación deben seguirse por al menos 2 meses a los voluntarios de la fase III”, insistió Laura Bover desde Texas, Estados Unidos.
Tres vacunas aprobadas contra el COVID-19
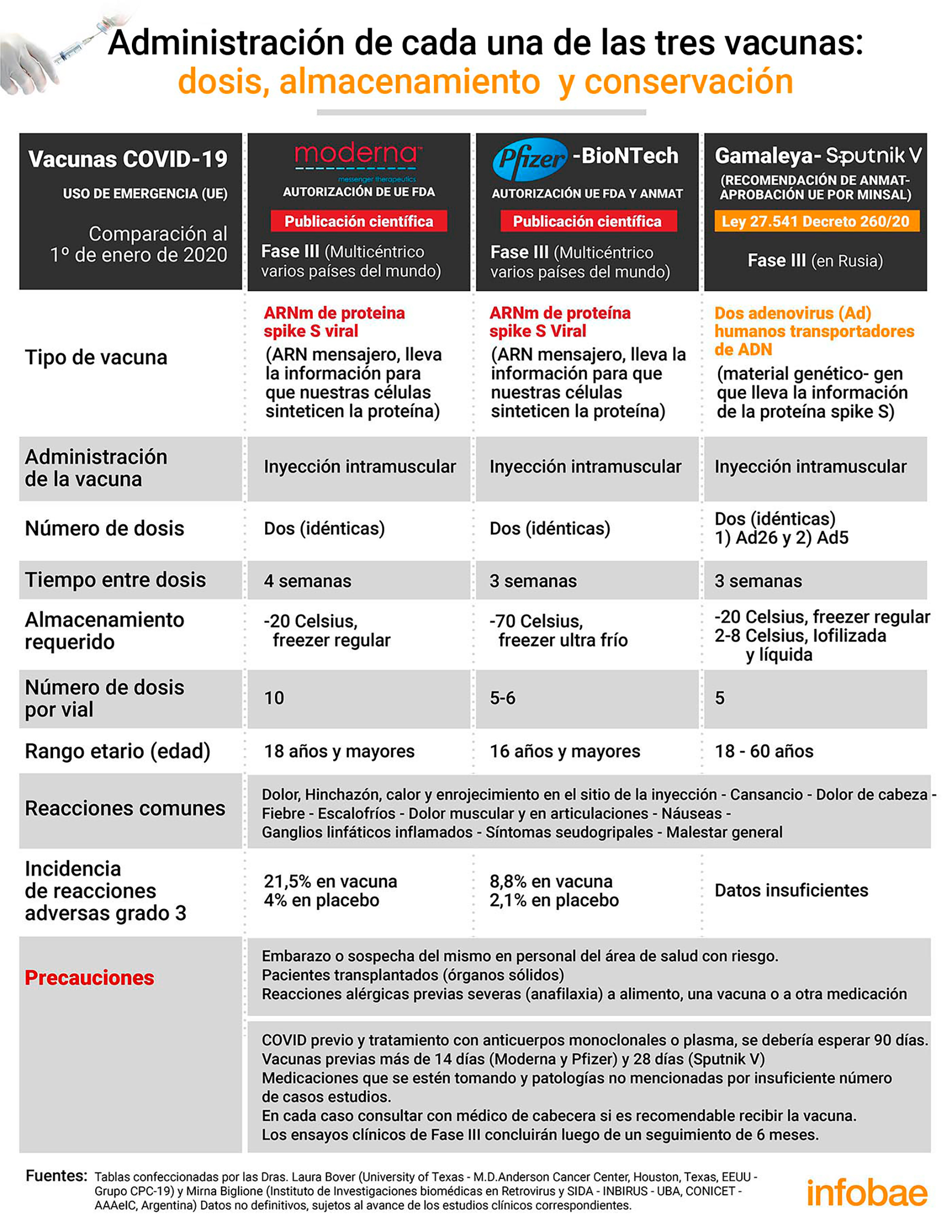
Tanto la vacuna de Moderna como la de Pfizer cuentan con tecnología ARNm de proteína spike S viral (ARN mensajero, lleva la información para que nuestras células sinteticen la proteína). Sputnik se vale de dos adenovirus (Ad) humanos transportadores de ADN (es decir material genético-gen que lleva la información de la proteína spike S).
Las 3 vacunas se administran a partir de una inyección intramuscular, en dos dosis idénticas en el caso de Moderna y Pfizer y dos diferentes (Ad26 y Ad5) en el caso de Sputnik V. Moderna tiene un tiempo entre dosis de 4 semanas mientras que Sputnik y Pfizer 3 semanas.
El almacenamiento requerido para Moderna es -20°C en freezer regular, Pfizer -70°C en freezer ultra frío y en Sputnik V -20 Celsius, freezer regular, 2-8 Celsius, liofilizada y líquida.

La vacuna de Moderna está pensada para un rango etario de mayores de 18 años, la de Pfizer para mayores de 16 y la de Gamaleya de 18 a 60 años.
Las reacciones adversas más comunes en los 3 casos fueron dolor, hinchazón y enrojecimiento en el sitio de la inyección, cansancio, dolor de cabeza, fiebre, escalofríos, dolor muscular y en articulaciones, náuseas, ganglios linfáticos inflamados, síntomas seudogripales y malestar general. En Moderna, 21,5% de los eventos adversos severos fueron en vacuna y 4% en placebo; en Pfizer 8,8% y 2,1% respectivamente y en Sputnik V los datos son insuficientes al 1 de enero de 2021.
Las precauciones a tener en cuenta en la de Moderna y Pfizer son ante embarazo o sospecha del mismo en personal del área de salud con riesgo, pacientes trasplantados (órganos sólidos) y ante reacciones alérgicas previas severas (anafilaxia) a alimentos, una vacuna, o a otra medicación. Para las 3 vacunas, las advertencias son para personas con COVID-19 previo y tratamientos con anticuerpos monoclonales o plasma, en donde se debería esperar 90 días, vacunas previas más de 14 días (Moderna y Pfizer) y 28 días (Sputnik V), medicaciones que se estén tomando y patologías no mencionadas por insuficiente número de casos estudiados y se aconseja en cada caso consultar con médico de cabecera si es recomendable recibir la vacuna. “Los ensayos clínicos de Fase III concluirían luego de un seguimiento de seis meses, en total dos años”, aseveraron.
El interior de las vacunas
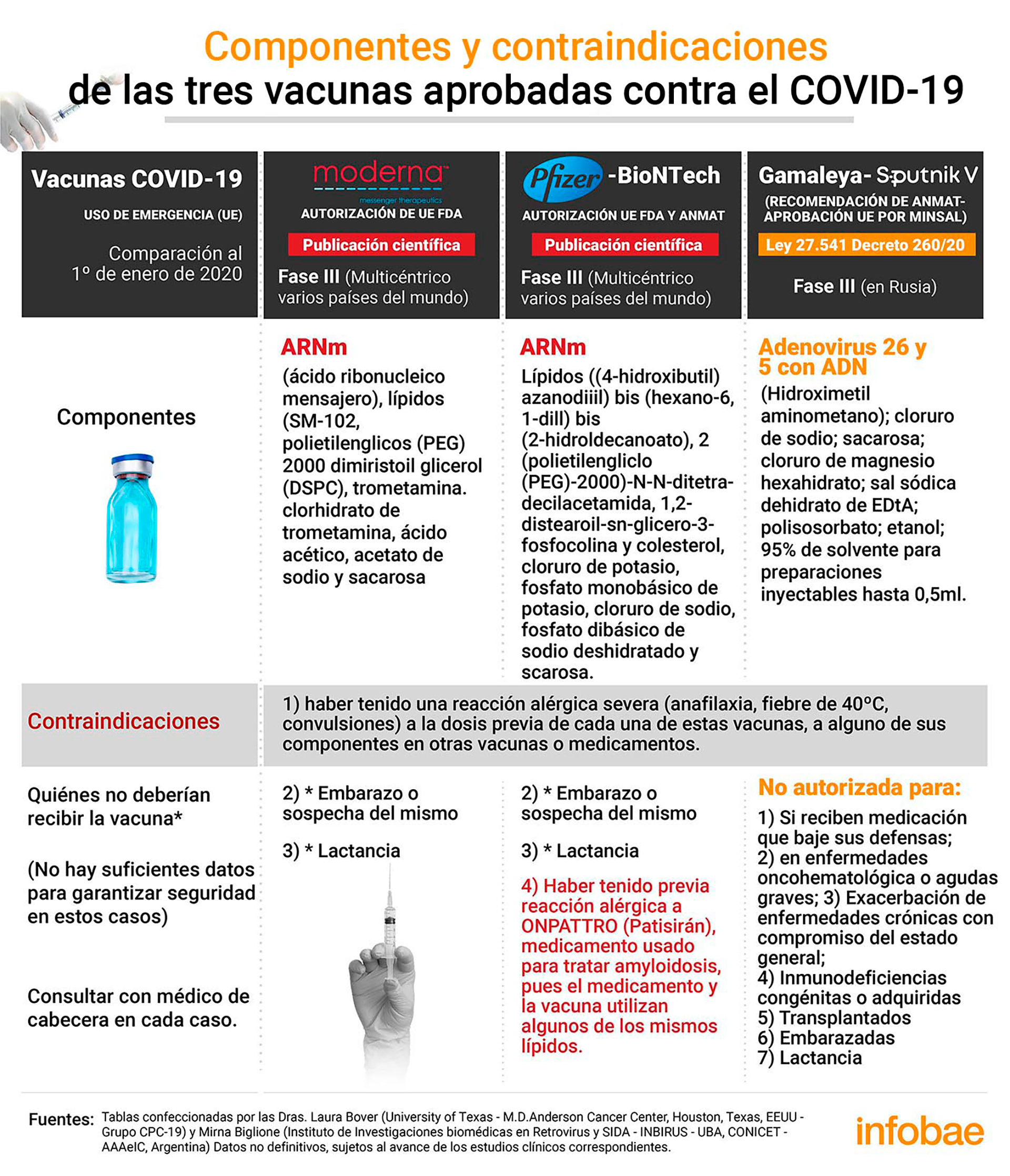
En cuanto a los componentes de las inoculaciones, la de Moderna está compuesta por ARNm (ácido ribonucleico mensajero), lípidos (SM-102, polietilenglicol [PEG] 2000 dimiristoil glicerol [DMG], colesterol y 1,2-diestearoil-sn-glicero-3-fosfocolina [DSPC]), trometamina, clorhidrato de trometamina, ácido acético, acetato de sodio y sacarosa.
Pfizer, por ARNm, lípidos ((4-hidroxibutil) azanodiil) bis(hexano-6,1-diil) bis(2- hidroldecanoato), 2 [(polietilenglicol [PEG]-2000]-N,N-ditetradecilacetamida, 1,2-distearoil-sn-glicero-3-fosfocolina y colesterol), cloruro de potasio, fosfato monobásico de potasio, cloruro de sodio, fosfato dibásico de sodio dihidratado y sacarosa.
En el caso de Sputnik V, Adenovirus 26 y 5 con ADN, Tris (hidroximetil aminometano); cloruro de sodio; sacarosa; cloruro de magnesio hexahidrato; sal sódica dihidrato de EDTA; polisorbato; etanol; 95 % de solvente para preparaciones inyectables hasta 0,5ml.
Máximas y contracara de inocular
De acuerdo a la recopilación de datos de las investigadoras Laura Bover y Mirna Biglione, quienes no deberían recibir la vacuna son aquellas personas que hayan tenido una reacción alérgica severa (anafilaxia, fiebre de 40°C, convulsiones) a la dosis previa de cada una de estas vacunas, a alguno de sus componentes en otras vacunas o medicamentos, en el caso de las 3 vacunas.
Embarazo o sospecha del mismo; lactancia en la de Moderna y Pfizer y en el caso particular de Pfizer/BioNTech aquellos que hayan tenido previa reacción alérgica al compuesto Onpattro (patisirán), medicamento usado para tratar amiloidosis, pues el medicamento y la vacuna utilizan algunos de los mismos lípidos.
Asimismo aclaran que Sputnik V no está autorizada para aquellos que reciben medicación que baje sus defensas; en enfermedades oncohematológicas o agudas graves; en exacerbación de enfermedades crónicas con compromiso del estado general; inmunodeficiencias congénitas o adquiridas; trasplantados; embarazadas y mujeres en procesos de lactancia.
Según amplió Bover a Infobae, “A principio de año todos decían que era una locura hacer una vacuna en 1 año. Ahora que está disponible, todos quieren la vacuna. Los 10-15 años que tarda en llegar a ser aprobada, se requieren para resolver todas esas dudas: quien la puede o no puede recibir, protege por cuantos meses o años, despierta inmunidad humoral (de anticuerpos) o celular (linfocitos T de memoria). Ahora hay que aprenderlo sobre la marcha. Lo que sabemos es que debe despertar los dos tipos de respuesta inmune: humoral (genera anticuerpos) y celular (linfocitos T de memoria)”.
“Los adenovirus que se usan como vectores transportando el gen de la proteína S del virus, en el caso de Sputnik son dos diferentes (Ad26 y Ad5). Eso es importante, porque si bien los adenovirus son utilizados como vectores (tipo transportador del ADN) esos dos no tienen mucha prevalencia (circulación) en la población. Los adenovirus son muy comunes y causan distintas enfermedades , resfríos, vías respiratorias, tracto digestivo. Estos como vectores no infectan, sólo llevan el material genético. Y al no ser muy comunes en la población y ser distintos adenovirus en cada dosis, probablemente sean menos rechazados por el sistema inmune que si dieran las dos dosis con el mismo. Porque el sistema inmune ya lo reconoció en la primera dosis y puede desencadenar la respuesta y eliminarlo antes que cumpla su función transportadora. Y al ser poco comunes en la población tenemos menos memoria inmunológica contra ellos”, precisó y detalló: “Esto representa una ventaja para la vacuna, que logrará su cometido de despertar una respuesta inmune contra la proteína S”.
“Es probable que todas las vacunas sean buenas y seguras, y eso se demostrará con el tiempo. Es posible que con gran número de vacunados los números de eficacia bajen del 90%, habrá quienes no desarrollen tanta protección. Pero lo más importante a recalcar, es que ninguna vacuna tiene eficacia del 100%. Eso indica que un 5-10% (o más) se pueden contagiar. Y tampoco se sabe si el que se contagie será asintomático, en cuyo caso puede tal vez contagiar a otro porque deja de cuidarse. Es por esto que lo más importante a comunicar es que hay que seguir cuidándonos”, concluyó Laura Bover a Infobae.
Infografías: Marcelo Regalado
SEGUÍ LEYENDO:
Últimas Noticias
Cuántos minutos de música son ideales para reducir la ansiedad, según un estudio clínico
Una investigación de la Universidad Metropolitana de Toronto planteó que esta intervención tiene beneficios para la salud en determinadas condiciones

Por qué sentirse solo genera más riesgo de enfermedades que el aislamiento real, según un estudio
Un análisis a largo plazo revela que quienes se sienten desconectados presentan mayor riesgo de patologías graves, independientemente de la cantidad de vínculos que tengan

La falta de hábitos de sueño constantes se asocia a mayor riesgo de obesidad y deterioro cognitivo, afirman expertos
Investigaciones recientes en adultos de distintos países muestran que quienes mantienen horarios irregulares de descanso presentan una probabilidad significativamente mayor de desarrollar problemas metabólicos y cognitivos, incluso cuando cumplen con el tiempo total de sueño recomendado

Por qué hacer ejercicio no siempre baja las calorías que pensamos
La adaptación corporal tras el esfuerzo físico puede modificar el funcionamiento metabólico e influir en otros procesos internos

Un estudio reveló que el consumo moderado de vino puede tener un efecto protector: cuáles son las razones
Una investigación en más de 340.000 adultos presentada en las sesiones científicas del Colegio Estadounidense de Cardiología mostró diferencias entre el tipo de bebida consumida y los riesgos para la salud. La palabra de los expertos a Infobae




