
Este domingo, el periodista de Radio Rivadavia Ricardo Benedetti dio a conocer en su cuenta de Twitter una copia de un supuesto documento interno de la Administración Nacional de Medicamentos, Alimentos y Tecnología Médica (Anmat) según el que la vacuna Sputnik V tuvo un total 12 eventos adversos serios al momento del análisis, tres de los cuales se dieron en adultos mayores de 60 años.
Infobae pudo confirmar con fuentes del organismo que el texto de cinco páginas fechado el 23 de diciembre a las 11.13.04 “es un informe del expediente” NO-2020-89948949-APN-DERM#ANMAT.
Así las cosas, el documento titulado Informe Dirección de Evaluación y Registro de Medicamentos, que lleva la firma de Nélida Agustina Bisio, analista técnico y titular de la Dirección de Evaluación y Registro de Medicamentos, expone parte de la información que aún no hizo pública el Fondo Ruso de Inversión Directa (RDIF, por sus siglas en inglés) sobre el total de voluntarios de Fase III que tuvieron efectos adversos y cuáles fueron los mismos.
El reporte contiene el análisis de los resultados correspondientes a 12.296 voluntarios de 18 a 87 años, de los cuales 9.258 recibieron la vacuna y 3.038 un placebo.
Según el texto, el evento adverso más frecuente observado fue un síndrome similar a la gripe en personas que recibieron la vacuna versus el placebo. Además, en total fueron reportados 12 eventos adversos serios, tres de los cuales ocurrieron en adultos mayores de 60 años, uno de los grupos de riesgo frente al SARS-CoV-2 y prioritario en la línea de vacunación después del personal médico.
Y tras detallar que los efectos no deseados son cólico renal, trombosis venosa profunda y un absceso en miembro, el informe asegura que no se reportaron los resultados de Fase III del análisis de inmunogenicidad, esto es, la capacidad que tiene un antígeno de activar el sistema inmunitario e inducir una respuesta inmune.
El documento, que va dirigido Marcelo Alberto Carignani, titular del Instituto Nacional de Medicamentos (INAME); y a Manuel Limeres, titular de la Anmat y su segunda al frente del organismo, Valeria Teresa Garay, no da cuenta sobre si los investigadores del Centro Nacional de Investigación de Epidemiología y Microbiología Gamaleya detuvieron la investigación para estudiar los casos de eventos adversos, tal como lo habían hecho en su oportunidad los laboratorios Pfizer y AstraZeneca en los ensayos de sus respectivas vacunas.
En el documento, asimismo se destaca: “El día 23 de diciembre en el marco de la Ley 27.573, esta Administración Nacional, elevó el informe de recomendación sobre la vacuna Sputnik V, al secretario de Calidad en Salud, doctor Arnaldo Medina, a los efectos de que el Ministerio de Salud de la Nación resuelva en virtud de sus facultades”.
“Los sujetos experimentaron efectos adversos serios (SAE por sus siglas en inglés) no relacionados con la vacuna basados en enfermedades preexistentes y documentadas antes del inicio del ensayo, incluida la enfermedad de cálculos renales, trombosis venosa profunda y absceso en una extremidad, causado por un desafortunado corte de uñas. Todas estas condiciones se han resuelto con éxito. Todos los SAE deben reflejarse de acuerdo con los requisitos de los procedimientos de los estudios clínicos, incluidos los que no están relacionados con la inoculación”, aseguró Denis Logunov, subdirector del Centro Gamaleya.

El informe llegó dos horas antes de que el Ministerio de Salud diera su autorización a la Sputnik V, atribución que se enmarca en la ley que aprobó el Congreso durante la pandemia, y allí la Anmat actúa “en el marco de sus competencias”, que es elevar un informe al Ministerio de Salud de la Nación con la recomendación de aprobar o no.
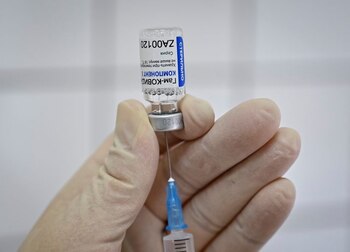
La comunicación de la decisión de la cartera sanitaria coincidió con el arribo de un avión de Aerolíneas Argentinas a Moscú para traer al país las primeras 300 mil dosis de la fórmula elaborada en Rusia, que finalmente hizo su llegada al país el 24 de diciembre y que ya están siendo distribuidas y comenzarían a ser aplicadas mañana martes.
“Las 300.000 dosis entregadas a Argentina son el primer componente de la vacuna. El segundo componente del Sputnik V se entregará en enero en total cumplimiento con el cronograma”, sostuvo Alexander Gintsburg, director del mismo centro.
SEGUÍ LEYENDO
Últimas Noticias
El consumo excesivo de sodio persiste como factor de riesgo clave para la insuficiencia cardíaca
Los hallazgos publicados en la revista “Journal of the American College of Cardiology: Advances” destaca la necesidad de fortalecer la prevención y mejorar el acceso a alimentos saludables para reducir complicaciones crónicas

Por qué los horarios irregulares de sueño influyen en los hábitos alimenticios y el sedentarismo adolescente
Investigadores advierten que dicha conducta se asocia a un mayor consumo de snacks, omisión del desayuno y menor actividad física, sobre todo cuando las rutinas escolares contradicen los ritmos biológicos

La alternativa natural a los suplementos proteicos: su presencia en la dieta, favorece el mantenimiento de la musculatura
Una revisión de evidencia científica demuestra que el aporte de proteínas vegetales y grasas saludables del cacahuete o maní puede representar una alternativa práctica y accesible frente a los complementos sintéticos convencionales

Cómo Gran Bretaña apuesta a la transición energética, el liderazgo climático y el desarrollo económico
En una entrevista exclusiva con Infobae, la ministra del Clima de Reino Unido explicó el impulso que su nación hace de la economía verde con políticas pioneras en la lucha contra el calentamiento global

PAMI adelanta su campaña de vacunación antigripal 2026 en todo el país: cuándo y cómo acceder
La decisión responde a la anticipación de la temporada de virus respiratorios y la circulación de una nueva variante de influenza A (H3N2)




