
Il laboratorio Moderna ha chiesto l'approvazione della Food and Drug Administration (FDA) degli Stati Uniti per una seconda dose di richiamo del vaccino COVID-19 per tutti gli adulti di età superiore ai 18 anni. Questo ordine copre molte più persone rispetto alla precedente domanda Pfizer/BioNTech per un'autorizzazione all'uso di emergenza per le persone di età superiore ai 65 anni.
La richiesta viene presentata nel bel mezzo di un acceso dibattito sulla durata della protezione dei vaccini contro il contagio e sulla necessità di dosi ripetute per prevenire malattie gravi e morte. Diversi paesi, come Israele, hanno iniziato a somministrare una quarta dose agli adulti e ci sono dati che mostrano che la produzione di anticorpi che combattono l'infezione è aumentata di cinque volte.
L'autorizzazione di una nuova dose del vaccino a RNA messaggero per tutti gli adulti fornirebbe «flessibilità» ai Centri statunitensi per il controllo e la prevenzione delle malattie (CDC) per decidere l'uso appropriato di una quarta dose, ha detto Moderna in una nota. Un accesso diffuso consentirebbe inoltre ai servizi sanitari di identificare su base individuale chi potrebbe beneficiare di una seconda dose di richiamo.
Gli esperti negli Stati Uniti ritengono che il caos nelle applicazioni di richiamo possa generare un dibattito disordinato e confuso su chi ha bisogno di una nuova dose e perché. Sia Moderna che Pfizer stanno anche testando una specifica dose di richiamo della variante Ómicron, i cui dati potrebbero essere disponibili entro settimane o mesi, creando la possibilità che le aziende possano chiedere l'approvazione normativa per uno specifico vaccino Omicron poco dopo l'attuale applicazioni della quarta dose.
Moderna non è entrata nei dettagli su quali informazioni sono state incluse nella sua domanda, se non dicendo che si basavano in parte su recenti dati statunitensi. e Israele sulla variante Omicron.
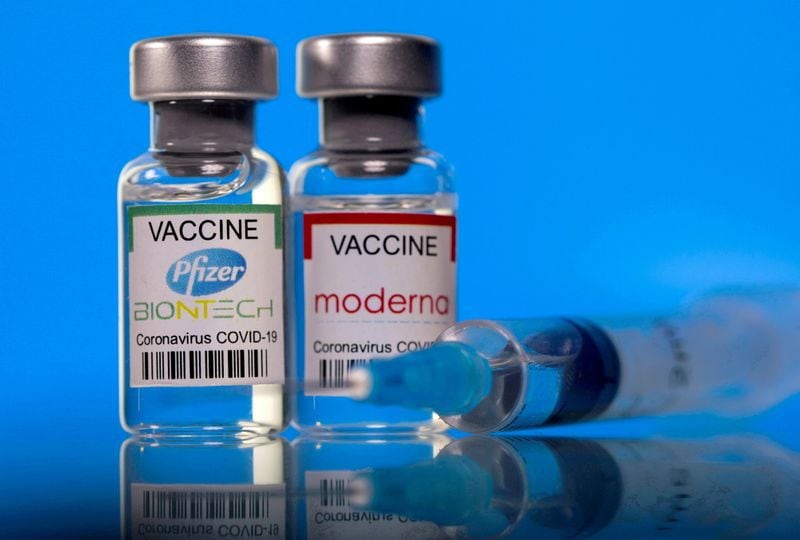
Pfizer, produttore dell'altro vaccino a RNA messaggero, ha chiesto l'autorizzazione per una seconda dose di richiamo per le persone anziane al fine di proteggere i più vulnerabili poiché l'immunità fornita dalle prime tre dosi diminuisce. Ha inoltre osservato di aver basato la sua richiesta su dati provenienti da Israele che concludono che somministrare una quarta dose agli anziani al culmine dell'onda Omicron ha contribuito a prevenire infezioni e casi gravi.
Studi e dati del mondo reale mostrano che la protezione di richiamo rimane forte contro malattie gravi e morte, ma diminuisce contro le infezioni dopo diversi mesi.
In una recente intervista, Anthony S. Fauci, direttore del National Institute of Allergy and Infectious Diseases, ha affermato che gli Stati Uniti finora, gli Stati Uniti mostrano che la protezione contro le malattie gravi rimane forte da quattro a cinque mesi dopo un richiamo, scendendo un po 'dall"efficacia del 91% nella prevenzione malattia grave al 78 percento.
La decisione della FDA in merito alla possibile applicazione di una quarta dose potrebbe arrivare in tempi relativamente brevi, soprattutto se i funzionari concludono che i dati sono semplici e non devono essere esaminati da un gruppo di esperti di vaccini esterni. I consulenti del CDC valuterebbero quindi chi dovrebbe essere idoneo per una seconda dose di richiamo e il direttore del CDC avrebbe l'ultima parola su tali raccomandazioni.
Il vaccino a due dosi Moderna ha ricevuto la piena approvazione della FDA per gli adulti lo scorso gennaio dopo aver ottenuto l'autorizzazione per l'uso di emergenza nel dicembre 2020 La FDA ha autorizzato un'iniezione di richiamo di vaccini a RNA messaggero a novembre.
«Le prove del mondo reale continuano a confermare l'efficacia e il forte profilo di sicurezza del vaccino Moderna COVID-19", ha affermato la società nella dichiarazione.
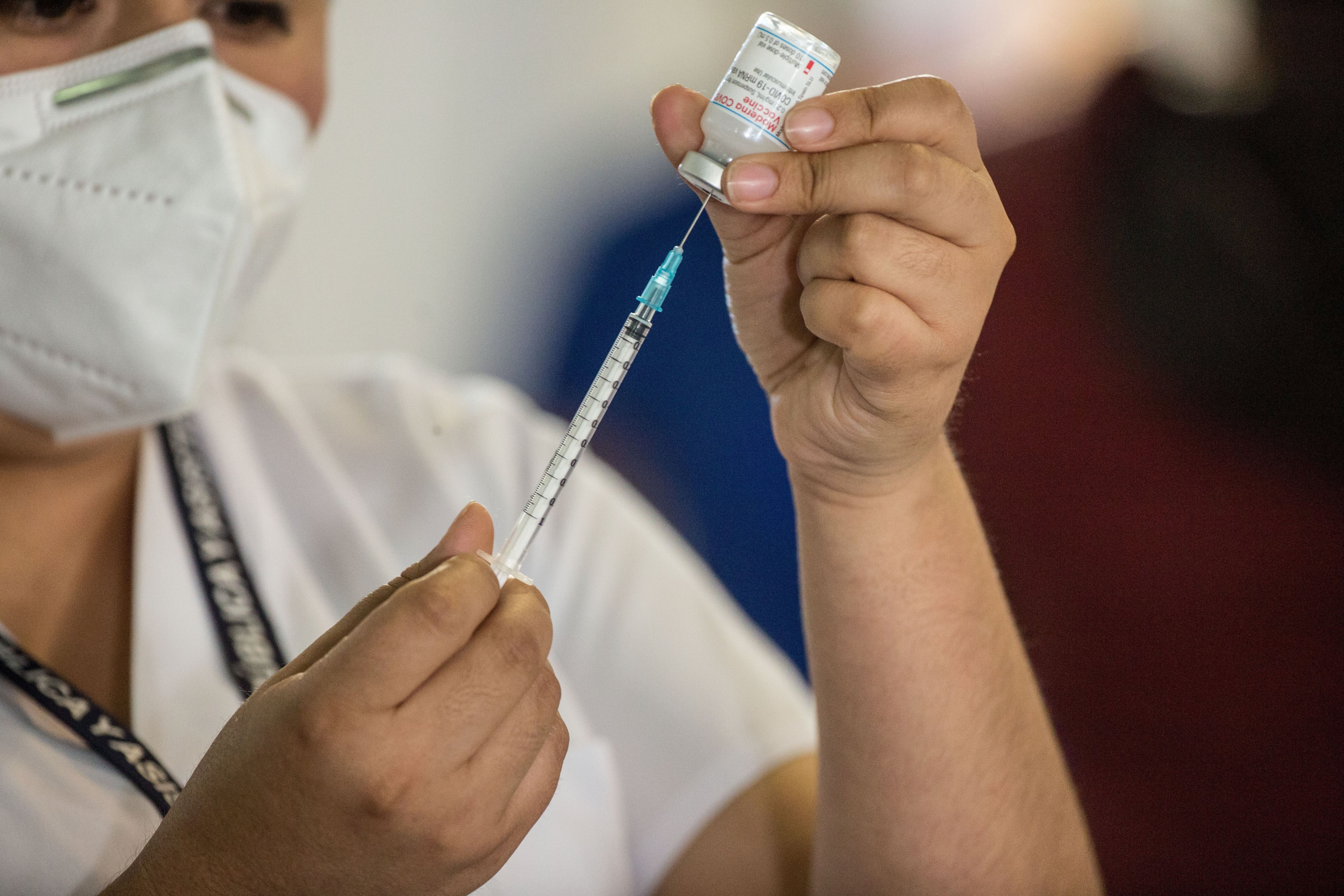
Un recente studio condotto da scienziati del Ragon Institute del Massachusetts General Hospital, dell'Università di Harvard, ha confermato l'efficacia dei booster dei vaccini a RNA messaggero contro la variante Omicron di COVID-19.
Secondo l'analisi pubblicata dagli specialisti sulla rivista Cell, le persone che sono state inoculate con le due dosi di Pfizer-BioNTech o Moderna e poi un booster hanno raggiunto una «potente» neutralizzazione contro la variante Ómicron. Lo stesso studio ha rilevato che il regime iniziale di vaccino a due dosi non produce anticorpi in grado di riconoscere e neutralizzare completamente la nuova variante scoperta in Sud Africa lo scorso novembre. Inoltre, hanno scoperto che contrarre l'infezione da Ómicron dopo essere stati vaccinati invece di essere stimolati non era altrettanto efficace. Il richiamo ha creato anticorpi «sostanzialmente più alti» rispetto alla vaccinazione seguita da infezione.
CONTINUA A LEGGERE
Más Noticias
Cortes de luz en Bogotá: estos barrios no tendrán servicio hoy, sábado 8 de marzo de 2025
Prográmese y evite inconvenientes por la intermitencia del servicio eléctrico en la capital colombiana

Se siente temblor de magnitud 4.4 en la ciudad de Sierra Gorda
En Chile los terremotos son una constante, incluso en el país ocurrió el mayor terremoto del que se tenga registro

Clima en Washington D. C.: cuál será la temperatura máxima y mínima este 8 de marzo
Para evitar cualquier imprevisto es importante conocer el pronóstico del tiempo

Pronóstico del clima en Miami este sábado: temperatura, lluvias y viento
Los fenómenos meteorológicos y análisis de probabilidad permiten dar información sobre la temperatura, lluvias y vientos para las próximas horas

Clima en Mérida: conoce el pronóstico y prepárate antes de salir
Debido a su ubicación geográfica, que le dan una gran variedad de climas, México es uno de los países con mayor biodiversidad y es hogar de al menos 12% de las especies del mundo

