
Cada vez está más cerca la línea de llegada en la prolífica carrera mundial para desarrollar una(s) vacuna(s) para proteger a las personas contra el nuevo coronavirus, SARS-CoV-2. Menos de un año después de que se identificó el virus en el labotarorio, casi 200 vacunas están en desarrollo, más de 40 están en ensayos clínicos, y solo seis vacunas transitan la Fase 3, la última etapa antes de lograr la aprobación de parte de los entes regulatorios. Todo esto gracias, a un esfuerzo mancomunado sin precedentes de investigadores de todo el mundo.
El más reciente informe de Nature sobre el progreso de la pandemia analiza los factores clave para que las vacunas sean seguras, eficaces y bienvenidas por el público.
Una vacuna segura y eficaz representa el arma más poderosa contra el virus, tanto a nivel individual como de población, pero no será la única. El uso de mascarillas, el lavado de manos y el distanciamiento social deberán continuar durante algún tiempo.
Al comienzo de la pandemia de coronavirus, los investigadores no entendían cómo podría desarrollarse la inmunidad natural al SARS-CoV-2. Pero eso cambió rápidamente. En cuestión de meses, los estudios habían demostrado que las personas infectadas pueden producir anticuerpos que neutralizan el virus, así como células T que pueden reconocer y matar las células infectadas con el virus.
Investigaciones posteriores han revelado que incluso las personas que no han sido infectadas con el virus pueden tener anticuerpos 3 y células T 2 que reconocen el SARS-CoV-2. Esto podría ser el resultado de que los individuos hayan sido previamente infectados con otros coronavirus como los que causan el resfriado común. Sin embargo, aún no se sabe si estas respuestas preexistentes brindan alguna protección contra la infección por SARS-CoV-2.
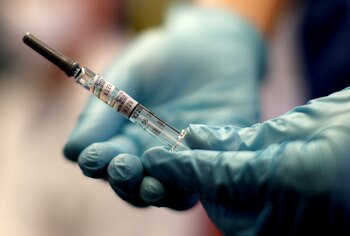
La presencia de estos anticuerpos y las respuestas de las células T fue una noticia prometedora para el desarrollo de vacunas: si la infección natural puede provocar este tipo de respuestas, entonces la vacunación podría provocar respuestas protectoras similares o más potentes.
La inmunidad implicada
La Administración de Drogas y Alimentos de los Estados Unidos (FDA) otorgó autorización de emergencia para un tratamiento llamado plasma convaleciente. Este implica administrar a las personas con COVID-19 plasma sanguíneo procedente de personas que se recuperan de la enfermedad, con el fundamento de que el plasma contiene muchos anticuerpos que reconocen el SARS-CoV-2. Sin embargo, el consenso entre médicos e investigadores es que la decisión de la FDA fue prematura porque no todos estos anticuerpos serían protectores.
Aún no hay evidencia definitiva de que este tratamiento sea efectivo, aunque se están realizando ensayos para explorar si el plasma convaleciente de personas con altos niveles de anticuerpos neutralizantes contra el virus podría ser beneficioso en el tratamiento pacientes en estado grave.
Un enfoque más prometedor que el plasma de convalecencia sería aislar anticuerpos neutralizantes específicos y potentes de los pacientes infectados y desarrollar tratamientos de anticuerpos basados en estos. Esta mirada ha tenido éxito para otras enfermedades virales: apenas la semana pasada, la FDA aprobó uno de esos tratamientos para el virus del Ébola. Y se están realizando ensayos para probar la eficacia de tales anticuerpos monoclonales contra COVID-19.

¿Qué tan cerca de una reinfección?
Otro interrogante urgente es si una persona que se ha recuperado del COVID-19 está protegida de futuras infecciones. Agosto dio a luz el primer informe confirmado de una persona reinfectada después de haberse recuperado; esto se determinó mediante la secuenciación de las cepas virales responsables de la infección original y la segunda. Desde entonces, ha habido un puñado de otros casos confirmados de reinfección por coronavirus, aunque en un contexto de más de 40 millones de infecciones en todo el mundo.
Las personas que se recuperan de otros tipos de infección por coronavirus pueden reinfectarse, porque las respuestas de anticuerpos en esos casos son relativamente breves. En el caso de COVID-19, aún no se sabe cuánto tiempo podría durar cualquier protección potencial; qué tan común es la reinfección; o hasta qué punto los individuos reinfectados no son detectados. En al menos dos de los casos documentados de reinfección, la enfermedad fue más grave la segunda vez, aunque los casos leves de reinfección pueden pasar desapercibidos.
Los estudios de autopsia indican que los centros germinales (estructuras en los ganglios linfáticos y el bazo donde las células B productoras de anticuerpos maduran y se diferencian) pueden estar ausentes en personas con COVID-19 grave, lo que provoca una pérdida de células B productoras de anticuerpos. Esto podría significar que la respuesta de los anticuerpos a la infección natural no es duradera.
Pero otros estudios en personas infectadas han mostrado evidencia de respuestas más duraderas: los anticuerpos alcanzan su punto máximo poco después de la infección y luego disminuyen cuando la infección ha desaparecido, permaneciendo en niveles más bajos a partir de entonces, al menos durante el período estudiado.
Entre los reinfectados se ha detectado otro punto de conflicto: las cepas no eran las mismas.
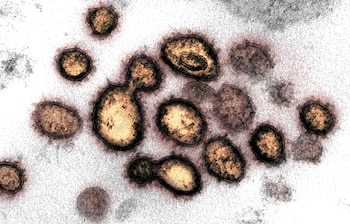
Gravedad e inmunidad
Una característica notable del COVID-19 grave es que la salud de las personas afectadas a menudo parece deteriorarse rápidamente durante la segunda semana de infección, en muchos casos después de síntomas inicialmente relativamente leves. Los primeros estudios de estos pacientes insinuaron una respuesta inmune desequilibrada, con una respuesta inflamatoria hiperactiva que no lograba controlar el virus y, en cambio, provocaba la enfermedad.
El fármaco dexametasona, que amortigua la respuesta inflamatoria y se usa ampliamente para tratar muchas afecciones inflamatorias, ha sido una de las pocas terapias efectivas para reducir la mortalidad por COVID-19 grave.
Un trabajo publicado el mes pasado mostró que al menos el 10% de los hombres y un porcentaje menor de mujeres con enfermedad grave tienen autoanticuerpos. Estos interfieren con la función de un grupo de proteínas conocidas como interferones, un componente crucial de la respuesta inmune antiviral.
A medida que el esfuerzo por desarrollar vacunas se acelera, será necesario responder preguntas clave para garantizar que sean seguras y efectivas.
En el lado positivo, el virus no parece estar mutando rápidamente, a diferencia de, por ejemplo, el virus de la influenza. Esto significa que el SARS-CoV-2 probablemente no mutará rápidamente para evadir una respuesta inducida por la vacuna. Al mismo tiempo, todavía no se sabe si la inmunidad inducida por la vacuna será de corta o larga duración, ni qué tan efectiva será una vacuna en las personas mayores, cuyos sistemas inmunológicos a menudo responden menos a la vacunación. Si la inmunidad es de corta duración, las poblaciones vacunadas necesitarán refuerzos regulares.

También llevará tiempo resolver una gran cantidad de cuestiones logísticas y de la cadena de suministro. La administración de vacunas requiere equipos como viales y agujas. En algunos países, es posible que sea necesario conservar las existencias en cámaras frigoríficas y, en muchos lugares, será necesario contratar y capacitar a más trabajadores de la salud. Luego está la cuestión de qué países –y qué grupos dentro de los países– deberían tener acceso prioritario. Varias organizaciones están trabajando para resolver estas cuestiones.
Las vacunas COVID-19 serán consideradas para su aprobación por la Organización Mundial de la Salud (OMS) bajo su lista de uso de emergencia, en la que se aprueba una vacuna para su uso mientras aún se están realizando los ensayos. La OMS y los reguladores nacionales están trabajando bajo una tremenda presión de los gobiernos y la industria farmacéutica, pero todas las partes han declarado que no puede haber atajos para la aprobación regulatoria. La confianza pública en las vacunas es esencial, por lo que se debe permitir que los reguladores completen su trabajo sin interferencias.
La vacilación ante las vacunas presenta nuevos desafíos. Cualquier nueva vacuna debe ser monitoreada cuidadosamente para detectar efectos adversos, especialmente en poblaciones vulnerables. Superar las dudas sobre las vacunas también requerirá una transparencia radical por parte de las compañías farmacéuticas y sus socios académicos.
Una vacuna que funcione es esencial, pero debe ser segura y eficaz, y debe distribuirse de manera equitativa y entre quienes más la necesitan. Hasta que llegue, y probablemente durante mucho tiempo después, las personas deben ceñirse a soluciones que funcionen (pruebas rigurosas, rastreo y aislamiento) y cambiar su comportamiento para ayudar a frenar la propagación del virus. Mientras tanto, con el rabillo del ojo habrá que hacer seguimiento a las cepas para que no hagan una mala jugada a la ansiada vacuna.
Encontrar la vacuna: una búsqueda científica que avanza a una velocidad récord

El esfuerzo mundial para crear una vacuna para el nuevo coronavirus comenzó en enero, poco después de que científicos en China publicaran en línea el genoma de un virus que causa una neumonía misteriosa. El desarrollo de vacunas suele llevar años y se desarrolla paso a paso. Los candidatos a vacunas experimentales se crean en el laboratorio y se prueban en animales antes de pasar a ensayos clínicos en humanos cada vez más grandes.
Estos pasos ahora se superponen en la carrera para encontrar una vacuna para una enfermedad global que ha matado a cientos de miles de personas. Las pruebas en humanos comenzaron en algunos casos antes de que terminaran los estudios en animales. A medida que las empresas lanzan pequeños ensayos de fase 1 destinados a establecer la dosis correcta, ya están planificando los ensayos de fase 3 que evalúan si las vacunas son efectivas y seguras.
No se están saltando pasos y las vacunas no se considerarán para su aprobación hasta después de un gran ensayo de fase 3. La Administración de Alimentos y Medicamentos de los Estados Unidos (FDA por sus siglas en inglés), que tiene la última palabra en el país sobre si una vacuna ha demostrado ser segura y efectiva, dice que una vacuna para el COVID-19, la enfermedad causada por el coronavirus, deberá prevenir la enfermedad o disminuir los síntomas en al menos un 50% de los que lo reciben. La eficacia de la vacuna contra la gripe varía del 40 al 60%, según los Centros para el Control y la Prevención de Enfermedades.

Otros países pueden usar estándares diferentes o autorizar vacunas sin esperar pruebas de que son seguras y efectivas. Rusia anunció que comenzaría a usar su vacuna en personas con alto riesgo de contraer el virus en agosto, antes de comenzar su ensayo de fase 3. China ha autorizado una vacuna para su uso en miembros del ejército. Y recientemente, la Agencia Europea de Medicamentos anunció que analizará los datos de la vacuna de Oxford-Astrazeneca en tiempo real mientras se lleva a cabo el ensayo de fase 3.
En enero, investigadores de Estados Unidos se fijaron un objetivo audaz de desarrollar una vacuna contra el coronavirus en un plazo de 12 a 18 meses. Este sería un récord mundial. Se considera que la vacuna contra las paperas es la más rápida en pasar, en cuatro años, del concepto científico a la aprobación en 1967. La búsqueda de una vacuna contra el VIH continúa, 36 años y contando.
Las vacunas contra el coronavirus se están moviendo mucho más rápido, en parte porque los gobiernos están asumiendo el riesgo financiero de desarrollar una vacuna que puede no funcionar. A través de Operation Warp Speed, el gobierno de EEUU ha invertido alrededor de USD 9.5 mil millones para acelerar el desarrollo y poner en marcha la fabricación antes de que finalice la investigación.
SEGUÍ LEYENDO:
Últimas Noticias
Los nuevos 60: los cambios en la dieta adulta que pueden agregar casi 10 años de vida
Los cambios en la dieta en la edad adulta pueden agregar casi 10 años de vida según un amplio estudio científico. Una guía de pequeños grandes hábitos para alcanzar la plenitud

9 tips para comenzar a hacer deporte y mejorar el estado físico
Una guía para evitar las excusas y ponerse en movimiento. Incorporar desafíos de manera paulatina y armar una rutina son los pasos claves para empezar

Día Mundial del Pene: cuidados para la higiene adecuada y consejos para prevenir el cáncer y otras enfermedades
La fecha busca celebrar la fertilidad y generar conciencia acerca de la práctica del sexo seguro. La salud y el cuidado del órgano reproductor masculino son fundamentales para mantener una vida sexual plena y saludable

Turbulencias durante el vuelo: cinco consejos para subirse al avión sin miedo
Un piloto comercial explica por qué son habituales estos movimientos, además brindó recomendaciones sobre qué asiento elegir para sufrir menos durante el viaje. Una guía práctica y sencilla sobre algunos de los puntos más consultados por los pasajeros

Cuáles son los tres desayunos ideales para personas con diabetes e hipertensión
Las clásicas tostadas con mermelada pueden reemplazarse por opciones más saludables, con más proteínas, fibras y minerales. Cómo ayudan a controlar estas enfermedades



