
Luego de que la Administración para la Alimentación y los Medicamentos de Estados Unidos (FDA, por sus siglas en inglés) anunciara el domingo 23 de agosto la autorización de las transfusiones de plasma con anticuerpos a enfermos de COVID-19, el Proyecto Nacional de Plasma Convaleciente COVID-19 (CCPP19), un grupo de médicos y científicos de 57 instituciones en 46 estados de Estados Unidos, emitió un comunicado expresando la gratitud y lo necesario que era contar con la autorización.
Desde el pasado mes de marzo la Administración para la Alimentación y los Medicamentos de Estados Unidos (FDA, por sus siglas en inglés) aprobó los ensayos con plasma para probar su efectividad y desde entonces se han realizado más de 60.000 tratamientos con plasma. Ahora, con la aprobación de emergencia, el tratamiento se extenderá al todo el país. “Hoy la FDA ha emitido una autorización de uso de emergencia de plasma para el tratamiento de la COVID-19 en pacientes hospitalizados en el marco de la lucha de la agencia contra la COVID-19”, informó la FDA en un comunicado.
“Recibimos y aceptamos la decisión de la FDA de poder brindar plasma convaleciente a pacientes enfermos de COVID-19. El plasma convaleciente aborda una brecha en las opciones terapéuticas que se avecina hasta que se pueda lograr una vacunación generalizada. Apreciamos el sano debate sobre cómo equilibrar la necesidad urgente con nuestro conocimiento de eficacia en medio de una nueva pandemia”, dicta el comunicado.

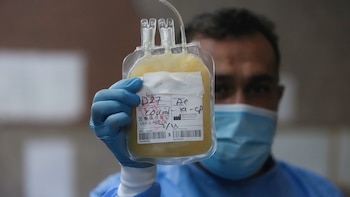
El tratamiento de plasma convaleciente, es una parte de la sangre que queda cuando, al extraerla, decantan los glóbulos rojos y blancos. La parte líquida, sin células, que suele ser de tono amarillo, es el plasma. Cuando una persona se infecta con un virus, patógeno o microorganismo que lo enferma la primera respuesta parte del sistema inmune. Este produce anticuerpos con las células de los glóbulos blancos. Hoy se transformó en una de las mejores armas contra la enfermedad COVID-19 que origina el nuevo coronavirus SARS-CoV-2, hasta tanto haya una vacuna eficaz para combatirlo.
En este sentido, el organismo que se autorganizo para velar por el tratamiento del plasma convalenciente en Estados Unidos, explicó que esperan que las lecciones aprendidas por el COVID-19 hagan que la humanidad esté mejor preparada por si en el futuro, otra pandemia golpea. “La experiencia con el uso de plasma contra COVID-19 ilustra la necesidad de tener protocolos de ensayos clínicos disponibles listos para usar para que puedan implementarse inmediatamente en lugar de tener que ser desarrollado y desplegado durante la crisis epidémica”, dicta el comunicado oficial.
A través del uso de plasma convaleciente de pacientes diagnosticados y recuperados de SARS-COV (coronavirus) los profesionales médicos pueden encontrar una herramienta terapéutica para los enfermos que actualmente luchan contra la infección.

De este modo, desde la CCPP19, explicaron que será interesante la administración del plasma convaleciente en los hospitales con escasez de personal ya que los requisitos reglamentarios alejaron a los médicos de la atención al paciente e introdujeron retrasos en la administración de plasma. Dada la evidencia disponible de que el plasma funciona mejor cuando se administra con anticipación, por este motivo, la nueva aprobación de la FDA puede eliminar las barreras para un uso óptimo”
El organismo basó la decisión en las pruebas científicas disponibles por las que “este producto podría ser eficaz para tratar la COVID-19 y se conocen los beneficios potenciales que compensan los riesgos potenciales y conocidos del mismo”.
Cifras que acompañan
Uno de las instituciones médicas líderes en la investigación de tratamientos contra el COVID-19 es Mayo Clinic. Sus investigadores ya han tratado a más de 20.000 pacientes con plasma experimental de convalecientes, afirmando que fue seguro después de la transfusión. Los resultados del programa para acceso ampliado en la COVID-19, perteneciente a la Administración de Alimentos y Medicamentos de Estados Unidos, constan en Mayo Clinic Proceedings.
El estudio realizado analizó los 7 días posteriores a las transfusiones realizadas entre el 3 de abril y el 11 de junio en pacientes hospitalizados, a quienes se los consideraba en riesgo de avanzar a un estado grave o mortal. De los pacientes, casi el 40 por ciento eran del sexo femenino, el 20 por ciento eran afroamericanos, casi el 35 por ciento era de origen hispano y el 5 por ciento era de origen asiático. Las tasas de mortalidad a los 7 días descendieron a 8.6 por ciento, desde el 12 por ciento mostrado en un estudio sobre seguridad previamente realizado en los primeros 5000 pacientes transfundidos. Los sucesos adversos graves continuaron por debajo del uno por ciento.
El informe ampliado sobre la seguridad revela un descenso en la mortalidad que parece coincidir simultáneamente con la disponibilidad más rápida de plasma para transfundir, aunque los autores advierten que esto en sí mismo no aporta ninguna evidencia sobre la eficacia del plasma de convalecientes para tratar la COVID-19. Dado el uso acelerado de la terapia, las investigaciones ahora se amplían para concentrarse en determinar qué indica su eficacia. Por el momento, el tratamiento con plasma de convalecientes es la única terapia basada en anticuerpos para la COVID-19.
“Tenemos una deuda de gratitud con la masiva red de base de donantes, organizadores, médicos profesionales, hospitales y bancos de sangre cuyos esfuerzos combinados desde marzo pasado han hasta ahora han trabajado en este tratamiento. Esperamos que este reciente desarrollo logre estimular el interés en la donación de sangre y plasma para combatir el COVID-19″, concluye el comunicado.
SEGUÍ LEYENDO
Últimas Noticias
Los nuevos 60: los cambios en la dieta adulta que pueden agregar casi 10 años de vida
Los cambios en la dieta en la edad adulta pueden agregar casi 10 años de vida según un amplio estudio científico. Una guía de pequeños grandes hábitos para alcanzar la plenitud

9 tips para comenzar a hacer deporte y mejorar el estado físico
Una guía para evitar las excusas y ponerse en movimiento. Incorporar desafíos de manera paulatina y armar una rutina son los pasos claves para empezar

Día Mundial del Pene: cuidados para la higiene adecuada y consejos para prevenir el cáncer y otras enfermedades
La fecha busca celebrar la fertilidad y generar conciencia acerca de la práctica del sexo seguro. La salud y el cuidado del órgano reproductor masculino son fundamentales para mantener una vida sexual plena y saludable

Turbulencias durante el vuelo: cinco consejos para subirse al avión sin miedo
Un piloto comercial explica por qué son habituales estos movimientos, además brindó recomendaciones sobre qué asiento elegir para sufrir menos durante el viaje. Una guía práctica y sencilla sobre algunos de los puntos más consultados por los pasajeros

Cuáles son los tres desayunos ideales para personas con diabetes e hipertensión
Las clásicas tostadas con mermelada pueden reemplazarse por opciones más saludables, con más proteínas, fibras y minerales. Cómo ayudan a controlar estas enfermedades




