
La Agencia Europea de Medicamentos (EMA) dio este miércoles su visto bueno al uso de la vacuna del laboratorio estadounidense Moderna contra el covid-19 en mayores de 18 años y la consideró lo suficientemente segura y eficaz. Unas horas después de la aprobación del ente regulador, la Comisión Europea otorgó una licencia de condicional para su uso en los países europeos.
El comité de medicamentos humanos (CHMP) concluyó de forma positiva su evaluación de todo el paquete de datos compartidos por Moderna, que incluía información sobre el proceso de producción, la calidad, los ingredientes, y los datos del ensayo clínico llevado a cabo por la farmacéutica.
“La EMA recomendó conceder una autorización de comercialización condicional para la vacuna covid-19 de Moderna para prevenir la enfermedad de coronavirus 2019 en personas a partir de los 18 años”, indicó la agencia con sede en Ámsterdam en un comunicado.
“Hemos autorizado la vacuna de Moderna, la segunda vacuna aprobada en la UE”, escribió horas después en Twitter la presidenta de la Comisión Europea, Ursula von der Leyen.
Los países del bloque europeo habían estado presionando a la EMA, para que autorizara la vacuna Moderna, ya que los casos de coronavirus se disparan en toda Europa. El regulador no pudo decidir sobre la aprobación en una reunión el lunes, que se había adelantado del 12 de enero, y los expertos tuvieron que reunirse de nuevo el miércoles. La EMA dijo que en el tiempo transcurrido había estado “trabajando duro para aclarar todos los asuntos pendientes con la compañía”.
La UE comenzó a vacunar el 27 de diciembre pero el ritmo ha sido lento, y el miércoles Holanda se convirtió en el último país del bloque en comenzar.
“Esta vacuna nos proporciona otra herramienta para superar la emergencia actual”, dijo el director ejecutivo de EMA, Emer Cooke. “Es un testimonio de los esfuerzos y el compromiso de todos los involucrados que tenemos esta segunda recomendación de vacuna positiva justo un año después de que la OMS declarara la pandemia”, añadió.
La jefa de la Comisión Europea, Ursula von der Leyen, dijo que era “una buena noticia para nuestros esfuerzos por llevar más vacunas Covid-19 a los europeos”.
La decisión de la EMA se ha basado en los resultados de un ensayo clínico con 30.000 personas de entre 18 y 94 años que no tenían signos de infección previa de Covid-19. En el mismo, se observó una reducción del 94,1 por ciento en el número de casos sintomáticos de Covid-19 en las personas que recibieron la vacuna, en comparación con las personas que recibieron inyecciones simuladas (185 de 14.073 personas).
Asimismo, el ensayo también mostró una eficacia del 90,9 por ciento en participantes con riesgo de Covid-19 grave, incluidos aquellos con enfermedad pulmonar crónica, enfermedad cardiaca, obesidad, enfermedad hepática, diabetes o infección por VIH. La alta eficacia también se mantuvo en todos los géneros, grupos raciales y étnicos.
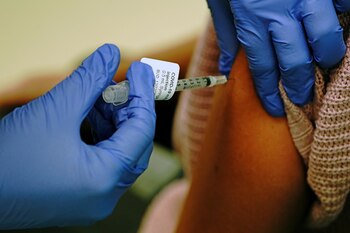
La vacuna de Moderna se administra en dos inyecciones en el brazo, con 28 días de diferencia. Los efectos secundarios más comunes de la vacuna han sido generalmente leves o moderados y mejoraron unos días después de la vacunación. Estos son dolor e hinchazón en el lugar de la inyección, cansancio, escalofríos, fiebre, ganglios linfáticos inflamados o sensibles debajo del brazo, dolor de cabeza, dolor muscular y articular, náuseas y vómitos.
(Con información de AFP, EFE y Europa Press)
MÁS SOBRE ESTE TEMA:
Últimas Noticias
Dos ex espías del Mossad revelaron cómo Israel engañó a Hezbollah con los dispositivos explosivos: “Creamos un mundo ficticio”

Roma pone límites al ritual de la Fontana de Trevi: las nuevas reglas tras su impactante renovación

El Vaticano se prepara para el histórico Jubileo 2025: fe, seguridad y millones de peregrinos

Genghis Khan mató a tantas personas que hizo que se enfriara el planeta

Cómo es el teleférico más empinado del mundo que acaba de inaugurarse en una zona emblemática de los Alpes



