
El Instituto de Investigación Biológica de Israel obtuvo hoy la autorización para iniciar el próximo 1 de noviembre los ensayos clínicos en humanos de la vacuna que desarrolla contra la COVID-19.
“Hace apenas dos meses recibí el primer frasco de la vacuna. Hoy ya contamos con 25.000 dosis y estamos comenzando la siguiente fase”, celebró Benny Gantz, el titular de Defensa, ministerio que supervisa el instituto (IIBR, por sus siglas en inglés).
El Ministerio de Sanidad y el llamado Comité de Helsinki, un organismo de expertos israelí que aprueba los experimentos en humanos, autorizaron hoy iniciar “la fase más crucial” del desarrollo de la vacuna israelí del coronavirus.
Dos participantes recibirán la vacuna el próximo domingo 1 de noviembre y, si el resultado es exitoso, se administrará a ochenta voluntarios de entre 18 y 55 años.
Posteriormente, se ampliarán a una segunda fase de 960 participantes en diciembre, con una tercera y última fase de 30.000 personas en abril o mayo, dependiendo de los resultados de las fases anteriores.
Los voluntarios estarán supervisados durante las primeras horas en los centros hospitalarios de Sheba, en Tel Aviv, y Hadassah de Jerusalén, tras lo que serán dados de alta y recibirán un seguimiento médico durante tres semanas.
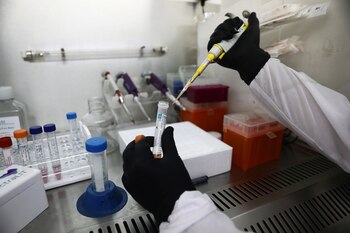
“Los científicos comprobarán los posibles efectos secundarios y controlarán si los voluntarios desarrollan anticuerpos contra el virus”, explicó el instituto en un comunicado.
Durante una segunda etapa, prevista para diciembre, los ensayos se ampliarán a 960 voluntarios mayores de edad en varios centros médicos de todo el país, con el objetivo de garantizar “las precauciones de seguridad, la dosis y la efectividad de la vacuna”.
En la tercera y última etapa, programada para los meses de abril y mayo de 2021, 30.000 voluntarios recibirán la vacuna y, en caso de ser efectiva, será aprobada para uso masivo.
“Creo en las habilidades de nuestros científicos y estoy seguro de que podemos producir una vacuna segura y eficaz. El nombre comercial es ‘BriLife’”, adelantó el director del IIBR, Shmuel Shapira.
El nombre de la vacuna responde a un juego de siglas entre el término “salud” en hebrero (briut), la abreviatura de Israel (il) y la palabra inglesa “life”, vida.
El objetivo final del Instituto es producir 15 millones de vacunas tanto para los ciudadanos israelíes como “los vecinos cercanos” de la región.
La vacuna desarrollada por el IIBR se basa en un virus existente (VSV, virus de la estomatitis vesicular) y ha sido probada con éxito en animales, en los que desarrolló una respuesta inmunitaria eficaz tanto en pequeños animales (ratones, hámsteres y conejos) como en grandes (cerdos).
Más de 40 candidatas a vacunas contra el coronavirus se encuentran en ensayos clínicos en todo el mundo, según la Organización Mundial de la Salud.
Israel, un país de aproximadamente 9 millones de habitantes, ha informado de más de 300.000 casos de COVID-19 y casi 2.400 muertes.
(Con información de EFE y AP)
MÁS SOBRE ESTE TEMA:
Últimas Noticias
Un grupo de senadores de Estados Unidos visita Taiwán en pleno debate por el aumento del gasto militar
La comitiva es encabezada por Jeanne Shaheen, del Partido Demócrata y el republicano John Curtis
El inicio de la primavera marca la llegada del apogeo de los cerezos en las ciudades japonesas
La concurrencia a parques y lugares emblemáticos aumenta notablemente durante la breve etapa en la que los pétalos adornan calles y templos, factor que se convierte en atracción para la población local y extranjeros
Crecer sin pantallas: el experimento social de una comunidad que desafía la era digital
Greystones es una comunidad irlandesa que impulsa un acuerdo colectivo para que los niños no tengan teléfonos inteligentes antes de la secundaria

Cierre del Estrecho de Ormuz: ¿los países del Golfo podrían desarrollar rutas alternativas?
La intensificación de los controles y peajes en la principal vía marítima ha producido una caída abrupta en el tránsito de petroleros, empujando a los gobiernos regionales a buscar opciones para garantizar los envíos de energía al extranjero
Una refinería de petróleo en el norte de Israel fue alcanzada por restos de un misil interceptado
Las explosiones y los fragmentos generaron humo denso y requirieron la movilización de bomberos y fuerzas de protección civil, quienes trabajaron para prevenir daños mayores y proteger a los trabajadores y habitantes




