
La Comisión Federal para la Protección contra Riesgos Sanitarios (Cofepris) emitió una alerta por la comercialización ilegal y falsificación de remdesivir, tratamiento para la atención de pacientes con COVID-19 de uso exclusivo de instituciones públicas del gobierno federal y estatal.
A través de un comunicado, la dependencia informó que se detectó la falsificación de cuatro nuevos lotes de remdesivir:
EN2005A2-B
EN2009D7-Q
CM2022F5
CA2023G5
Lo anterior, como resultado de la “constante vigilancia sobre productos regulados por esta autoridad sanitaria y en seguimiento a la alerta emitida en julio de 2021″.

Además, Cofepris identificó productos con denominaciones distintivas como corovir, bemsivir, desrem, remdesivir, que no están autorizados para su comercialización y distribución en México.
¿Qué riesgos implican los lotes falsificados de remdesivir?
De acuerdo con la Comisión Federal para la Protección contra Riesgos Sanitarios, el riesgo de consumir medicamentos ilegales y falsificados radica en la falta de pruebas sobre la seguridad de sus ingredientes.
Así como en la inocuidad de su elaboración y el correcto almacenaje y distribución. Por ello, Cofepris recomendó no comprar fármacos que son de uso de emergencia o cualquier otro que se comercialice de manera irregular.
¿Cómo se puede detectar el remdesivir falsificado?
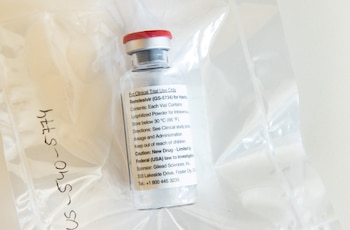
Según detalló la Cofepris, los lotes falsificados de remdesivir cuentan con características que permiten su identificación, entre ellas:
Tapa color azul y grabado
Leyendas y tipografía no autorizada para México
Presentación en sustancia líquida
Lotes no utilizados por Gilead Sciences
Tras la detección de los lotes, la Comisión Federal hizo un llamado a distribuidores autorizados, personal médico, clínicas y hospitales públicos que cuenten con stock del tratamiento, verificar que no pertenezcan a los lotes EN2005A2-B, EN2009D7-Q, CM2022F5 y CA2023G5.

“De contar con dichos lotes irregulares en almacén, se debe suspender de manera inmediata el suministro y presentar la denuncia correspondiente en la página de Cofepris”, se lee en el comunicado.
La dependencia agregó que el fármaco original fue aprobado en marzo de 2021 por la autoridad sanitaria bajo el esquema de uso de emergencia, por lo que sólo podrá suministrarse de forma gratuita en las instituciones públicas que conforman el Sistema Nacional de Salud y alta especialidad. De no ser así, la autoridad sanitaria podrá aplicar las sanciones administrativas pertinentes.
Cofepris alertó por 8 nuevos distribuidores irregulares de medicamentos
La Comisión Federal para la Protección contra Riesgos Sanitarios informó que actualizó la lista de distribuidores irregulares de medicamentos, en donde se detectó 8 nuevos distribuidores de medicamentos que incumplen con la regulación sanitaria del país.
De acuerdo con la dependencia, los siguientes distribuidores no garantizaron la “seguridad, calidad y eficacia de los medicamentos”:
- Mundo de Vacunas, SA de CV
- Proveedora de Medicamentos del Centro, SA de CV
- Proveedora y Distribuidora de Medicamentos Gaat, SA de CV (Farmacia Gaat)
- Access Pharma
- Suministros Biomédicos GDL
- RRA and BE Logistica de Mexico S.A.
- OTC Medicamentos Rolando Lugo
- Farmacia Bacort.
Asimismo, entre las irregularidades detectadas se encuentra el no contar con aviso de funcionamiento y que las actividades del domicilio no corresponden con el giro señalado, “lo que fue un obstáculo para que esta autoridad sanitaria supervisara las condiciones sanitarias de los establecimientos”.
Además, la dependencia dio a conocer que dos distribuidores fueron eliminados de la lista en la reciente actualización, debido a que se han regularizado y cumplen lo requerido por la Alta Directiva Sanitaria.
SEGUIR LEYENDO:
Más Noticias
La historia de “El Mencho”: cómo el líder del CJNG se convirtió en uno de los narcotraficantes más buscados en el mundo
Nemesio Oseguera Cervantes dirigió la organización criminal al menos desde el año 2000 y logró expandirlo a la mayoría de los estados de México y a varias ciudades de los Estados Unidos

700 años de Tenochtitlan: cómo un pueblo errante y repudiado se convirtió en el poderoso imperio de América
La fascinante la historia de cómo un puñado de personas con un sueño buscaron su identidad, fueron obligados a vivir en un islote marginal y lograron alianzas poderosas en el continente

La mujer que dobló al sistema y llevó el feminicidio a la SCJN para hacer justicia por su hija, que no se suicidó
La incansable lucha de Irinea Buendía hizo que las autoridades judiciales reconocieran la negligencia del caso de su hija Mariana Lima, pero además la gravedad del problema y las omisiones de las autoridades

David Alfaro Siqueiros en la prisión de Lecumberri: vida y obra del muralista en el “Palacio Negro”
El artista fue detenido acusado de disolución social y del intento de asesinato de Trotski. Esta es la historia poco conocida de su etapa como interno en una de las prisiones más duras en la historia

Qué es la meningitis, cuáles son sus síntomas y cómo tratarla
En algunos casos, esta enfermedad mejora sin tratamiento en algunas semanas, pero en otros pueden poner en riesgo la vida y requerir tratamiento con antibióticos de emergencia




