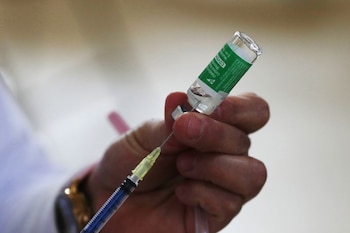
En fechas recientes, la Comisión Federal para la Protección contra Riesgos Sanitarios (Cofepris), la Secretaría de Seguridad Ciudadana (SSPC) y la Secretaría de Salud de Nuevo León informaron sobre la venta de vacunas falsas Pfizer-BioNTech.
De acuerdo con las dependencias, los productos encontrados en el lugar tenían el lote 783201 con fecha de caducidad en agosto de 2024. No obstante, se confirmó que son apócrifos.
Por su parte, el doctor Manuel de la O Cavazos reveló que supuesto antígeno habría sido aplicado, por lo menos, a 80 habitantes de una zona residencial en el estado. Ésta les habría costado desde 11,110 pesos en el caso más barato, hasta 25 mil pesos y en algunos casos, hasta 40 mil pesos.
Rosa Icela Rodríguez, titular de la SSPC, informó ó a través de un comunicado la detención de seis personas presuntamente involucradas con este delito, misma que efectuaron autoridades de Nuevo León.
En este sentido, la Cofepris recomendó que, en caso de haber sido adquirida la vacuna en este u otro establecimiento, habría de, primero, denunciarse ante las autoridades correspondientes a través de la página de internet oficial del gobierno federal: http://tramiteselectronicos03.cofepris.gob.mx/DenunciaExterna/W/InicioW.aspx
Y en caso de presentar reacciones adversas o malestares relacionados con la aplicación del biológico adjudicado a la empresa farmacéutica Pfizer-BioNTech, es necesario reportarlo a través de eReporting, VigiFlow o enviando un correo electrónico a farmacovigilancia@cofepris.gob.mx.
De acuerdo con la página oficial de la Cofepris, el sistema de notificación de reacciones adversas constituye la base de la farmacovigilancia, mediante la cual se pueden detectar, evaluar, comprender y prevenir los riesgos asociados a los medicamentos y vacunas.
Es a través del Centro Nacional de Farmacovigilancia donde se cuenta con un formato de notificación estandarizado que permite colectar la información necesaria para la notificación.
El compromiso de las autoridades es fortalecer el Programa Internacional para el Monitoreo de Medicamentos de la Organización Mundial de la Salud (OMS), mismo que opera a través del Centro de Monitoreo de Uppsala (UMC, por sus siglas en inglés) que alimenta la base de datos mundial de la seguridad de los medicamentos.
El primer método, E-Reporting, consiste en la notificación en línea por parte de pacientes/consumidores y Profesionales de la salud. Para solucionar dudas sobre su llenado, se puede consultar también el instructivo para la notificación de reacciones adversas (malestares ocasionados por los medicamentos).
Adicionalmente, los pacientes/consumidores de medicamentos tienen a su disposición el Formato para el Aviso de Sospechas de Reacciones Adversas de Medicamentos COFEPRIS-04-017 para notificar una sospecha de reacción adversa.

Aunado a esto, existe VigiFlow en los Centros Estatales de Farmacovigilancia (CEFV), Centros Institucionales de Farmacovigilancia (CIFV), Centros Institucionales Coordinadores de Farmacovigilancia (CICFV) y las Unidades de Farmacovigilancia (UFV) dependientes de los CEFV y los CICFV que cuenten con los medios electrónicos para el reporte utilizarán VigiFlow como canal para la notificación.
Para obtener más información sobre el uso de VigiFlow, es necesario consultar la Guía de farmacovigilancia para la notificación de cualquier problema de seguridad relacionado con el uso de medicamentos.
Por último, puedes enviar tu reporte para darle seguimiento a través de la página farmacovigilancia@cofepris.gob.mx, de acuerdo con la página oficial de la Cofepris.
MÁS SOBRE ESTE TEMA:
Más Noticias
La historia de “El Mencho”: cómo el líder del CJNG se convirtió en uno de los narcotraficantes más buscados en el mundo
Nemesio Oseguera Cervantes dirigió la organización criminal al menos desde el año 2000 y logró expandirlo a la mayoría de los estados de México y a varias ciudades de los Estados Unidos

700 años de Tenochtitlan: cómo un pueblo errante y repudiado se convirtió en el poderoso imperio de América
La fascinante la historia de cómo un puñado de personas con un sueño buscaron su identidad, fueron obligados a vivir en un islote marginal y lograron alianzas poderosas en el continente

La mujer que dobló al sistema y llevó el feminicidio a la SCJN para hacer justicia por su hija, que no se suicidó
La incansable lucha de Irinea Buendía hizo que las autoridades judiciales reconocieran la negligencia del caso de su hija Mariana Lima, pero además la gravedad del problema y las omisiones de las autoridades

David Alfaro Siqueiros en la prisión de Lecumberri: vida y obra del muralista en el “Palacio Negro”
El artista fue detenido acusado de disolución social y del intento de asesinato de Trotski. Esta es la historia poco conocida de su etapa como interno en una de las prisiones más duras en la historia

Qué es la meningitis, cuáles son sus síntomas y cómo tratarla
En algunos casos, esta enfermedad mejora sin tratamiento en algunas semanas, pero en otros pueden poner en riesgo la vida y requerir tratamiento con antibióticos de emergencia




