La tecnología del ARN se considera una de las fronteras más recientes de la medicina, pero, de hecho, un innovador primordial la alcanzó mucho antes que nosotros. El parásito de la malaria, un antiguo organismo unicelular, ha utilizado sofisticadas maniobras de ARN durante milenios. En un estudio publicado recientemente en Cell Reports , investigadores del Instituto de Ciencias Weizmann descubren las estrategias de ARN del parásito, mecanismos que podrían inspirar aplicaciones inesperadas para las herramientas basadas en ARN en diversas áreas de la medicina.
Hace más de una década, la profesora Neta Regev-Rudzki descubrió que el parásito de la malaria, Plasmodium falciparum, que invade los glóbulos rojos humanos, envía diminutas vesículas para comunicarse con otros parásitos dentro de otros glóbulos rojos. Se demostró que estas nanovesículas (envolturas en forma de saco dirigidas a otras células) transfieren fragmentos de ADN de un parásito a otro. Sin embargo, Regev-Rudzki y su equipo descubrieron que las vesículas también contienen otra carga molecular, incluyendo varios tipos de ARN.
Los investigadores razonaron que el astuto parásito no transportaría sus ARN mediante vesículas sin una buena razón. En el nuevo estudio, el equipo, del Departamento de Ciencias Biomoleculares de Weizmann, se propuso determinar si las vesículas permiten que los ARN realicen funciones más allá de la mensajería. Dado que el equipo había demostrado previamente que las nanovesículas penetran no solo en los glóbulos rojos, sino también en las células inmunitarias llamadas monocitos, los investigadores sospecharon que el parásito podría estar intentando alterar las defensas inmunitarias del huésped.

Pronto descubrieron que el parásito es aún más astuto de lo que imaginaban. El equipo, dirigido por la Dra. Paula Abou Karam, entonces estudiante de doctorado, descubrió que los ARN de las vesículas no eran fragmentos aleatorios, sino ARN mensajero, o ARNm; concretamente, moléculas que contienen instrucciones para producir una de las familias de proteínas más abundantes del parásito. ¿Podrían los parásitos estar insertando su propio ARNm en la maquinaria de producción de proteínas de las células en el citoplasma?
“Esto parecía increíble. La célula protege celosamente su núcleo porque alberga su ‘cerebro’”
Contrariamente a lo esperado, no se encontraron indicios de las proteínas parasitarias que esperaban que estos ARN produjeran en el citoplasma de los monocitos. En cambio, para sorpresa de los investigadores, los ARN parecían estar penetrando en los núcleos altamente protegidos de las células inmunitarias.
“Esto parecía increíble”, recuerda Regev-Rudzki, “la célula protege celosamente su núcleo porque alberga su ‘cerebro’. Para convencernos a nosotros mismos, y a los demás, de que los ARN del parásito realmente penetran estas defensas, tuvimos que observarlos directamente dentro del núcleo”.

Al principio, esta tarea parecía casi imposible. Las moléculas de ARN parasitarias están presentes en cantidades extremadamente pequeñas que se pierden fácilmente dentro del núcleo abarrotado. Otra dificultad radicaba en el propio genoma del parásito, que es inusualmente repetitivo, compuesto principalmente por solo dos letras genéticas, A y T. Por lo tanto, diseñar un método lo suficientemente sensible como para detectar el ARN del parásito entre todo el material genético del huésped fue un gran desafío.
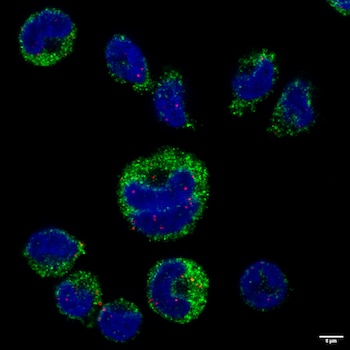
Alerta roja, pistas falsas: moléculas de ARN de la malaria (puntos rojos) observadas dentro de los núcleos (azules) de los monocitos (verdes) mediante microscopía confocal de fluorescencia.
“A veces, lo que determina el éxito o el fracaso de un proyecto de investigación es el estudiante que lo dirige, y este fue uno de esos casos clásicos”, dice Regev-Rudzki. “Paula aceptó el reto y perseveró durante un año y medio hasta que finalmente lo logró”.
Abou Karam desarrolló una sonda fluorescente que hacía que minúsculos puntos rojos se iluminaran dentro del núcleo del monocito. Cada punto representaba una molécula de ARNm de la malaria que había traspasado la barrera nuclear.
La siguiente pregunta fue: ¿Qué hacían allí estos ARN? Los investigadores descubrieron que, una vez dentro del núcleo, el ARNm del parásito se une a dos proteínas humanas, ACIN1 y PNN, componentes clave de la maquinaria de empalme celular. Al igual que la película de empalme, las células utilizan el empalme para editar las transcripciones de ARN, cortando y reorganizando segmentos antes de permitir que se traduzcan en proteínas. Sirve como un paso crucial de control de calidad: sin un empalme adecuado, los ARN no tienen sentido y, por lo general, se descartan antes de que puedan traducirse en proteínas.

En esta etapa, los investigadores unieron fuerzas con el equipo del Dr. Zeev Melamed , de la Universidad Hebrea de Jerusalén, experto en empalme y ARN. Juntos, revelaron la manipulación del empalme en monocitos receptores, descifrando así la estrategia del ARN del parásito.
Sabotaje en el núcleo
En efecto, el parásito interfiere con las comunicaciones internas del sistema inmunitario del huésped. Al introducir su ARNm en los núcleos de los monocitos, interrumpe el procesamiento del ARN de la propia célula huésped. El resultado es un caos. Las transcripciones inmunitarias esenciales, destinadas a producir proteínas que combaten las infecciones, se empalman incorrectamente y luego se envían para su degradación. Como resultado, se detiene la producción de familias enteras de proteínas inmunitarias.
A medida que observaban la toma de control de las células inmunitarias, los científicos descubrieron que los monocitos manipulados emitían señales de socorro, lo que desencadenaba una ola de activación inmunitaria que movilizaba más células inmunitarias. Pero mientras estas células se apresuraban a afrontar la aparente crisis dentro de los monocitos, la verdadera amenaza —los parásitos que se multiplican silenciosamente dentro de los glóbulos rojos— pasaba desapercibida.
“Es un mecanismo de señuelo”, dice Regev-Rudzki. “Como lanzar una granada en una dirección para que los guardias corran hacia ella, mientras tú te mueves a otra”. Al confundir a las células inmunitarias y suprimir proteínas de defensa clave, el parásito gana tiempo valioso para crecer y propagarse.
Estos hallazgos apuntan a un nuevo objetivo potencial para los fármacos antipalúdicos: terapias diseñadas para impedir que los ARN de la malaria alteren la maquinaria de empalme del huésped.
El trabajo también podría abrir nuevas vías para el diagnóstico, no solo de la malaria, sino también de otras enfermedades infecciosas. Los parásitos de la esquistosomiasis, por ejemplo, pueden residir en el intestino durante años, causando daños y permaneciendo indetectables en los análisis de sangre estándar. Regev-Rudzki cree que estos, y otros parásitos, podrían estar liberando vesículas cuyas firmas de ARN en el torrente sanguíneo podrían revelar su presencia.
Las implicaciones del estudio van mucho más allá de las enfermedades infecciosas. Las vesículas abundan en el cuerpo, y buscar su carga no solo en el citoplasma, sino también en lugares inesperados, como los núcleos, cuidadosamente protegidos, puede aumentar las posibilidades de interceptar estos paquetes y leer su ARN mensajero. Esto, a su vez, podría ayudarnos a descifrar los mecanismos que promueven la enfermedad. Las estrategias empleadas por el cáncer, por ejemplo, incluyen la liberación de vesículas que influyen en el tejido sano circundante. Las vesículas también son un área activa de investigación en el párkinson, la esclerosis lateral amiotrófica (ELA) y otras enfermedades neurodegenerativas. El ARN unido a vesículas que circula en la sangre podría algún día servir como biomarcadores tempranos para estos trastornos.
<br>
También participaron en el estudio Edo Kiper, Shaked Yadid, la Dra. Ewa Kozela, Nir Zharoni, la Dra. Reinat Nevo, Daniel Alfandari, Helina Otesh, Abel Cruz Camacho y el Dr. Ofer Shoshani del Departamento de Ciencias Biomoleculares de Weizmann; la Dra. Tamar Ziv del Technion – Instituto Tecnológico de Israel; el Dr. Yoav Lubelsky y el Prof. Igor Ulitsky del Departamento de Inmunología y Biología Regenerativa de Weizmann; los Dres. Ron Rotkopf, Ekaterina Petrovich-Kopitman y Ziv Porat del Departamento de Instalaciones Básicas de Ciencias de la Vida de Weizmann; el Dr. Eviatar Weizman del Centro Nacional de Medicina Personalizada Nancy y Stephen Grand Israel; Moshe Cossin de la Universidad Hebrea de Jerusalén; la Dra. Irit Rosenhek-Goldian del Departamento de Apoyo a la Investigación Química de Weizmann; y el Prof. Carmit Levy de la Universidad de Tel Aviv.
Últimas Noticias
Por qué los camellos pueden ver durante las tormentas de arena: la adaptación ocular que protege sus ojos
Un informe del biólogo evolutivo Scott Travers para Forbes describió cómo la anatomía de estos animales les permite superar los retos del desierto, manteniendo su orientación y seguridad frente a amenazas invisibles en su entorno

Un insecto tropical asombra a la ciencia por cambiar de color para camuflarse en la selva
El descubrimiento de un grillo capaz de modificar su tonalidad desconcierta a la comunidad científica y revela mecanismos insospechados de mimetismo en los ecosistemas selváticos

Una terapia experimental logró “interceptar” el cáncer de páncreas al detectar lesiones precursoras del tumor
Un estudio preclínico en ratones y publicado en Science mostró que eliminar lesiones microscópicas triplica la supervivencia de los pacientes
Científicos hallan hielo seco alrededor de una nebulosa en el espacio: qué revela sobre las estrellas
A 3.400 años luz de la Tierra, lograron identificar dióxido de carbono congelado en un denso anillo de polvo sometido a temperaturas extremas

Científicos estudian el impacto de rayos cósmicos: claves para proteger a astronautas en misiones espaciales
La nueva infraestructura científica desarrollada en Alemania brinda herramientas precisas para estudiar los efectos sobre organismos y materiales fuera de la órbita baja terrestre




